
【题目】下图所示为实验室常见气体制备、净化、干燥和收集的部分仪器。
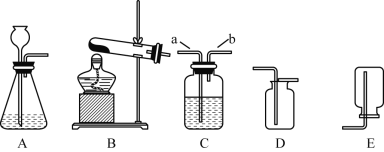
(1)某同学打算用高锰酸钾制取并收集干燥的气体,则可选择上述装置中_____(填字母序号),写出该反应的化学方程式_____。
(2)若打算制取二氧化碳,则发生装置应选择_____(填字母序号),在C装置中装入浓硫酸来干燥制取的气体,则应该从_____(填“a”或者“b”)端通入气体。
(3)用上述制取二氧化碳实验后的残留液进行pH检测、过滤、蒸发的操作训练。
①对固体残留物进行过滤,除了需要玻璃棒和烧杯外,还需要的玻璃仪器是_____;
②用pH试纸检测滤液的酸碱度,检测pH的操作方法是:把一片pH试纸置于干燥洁净的表面皿上,_____;测得溶液pH=4,说明有_____剩余。
③取上述少量滤液进行蒸发,蒸发过程玻璃棒不断搅拌的作用是_____。
【答案】BD ![]() A a 漏斗 用玻璃棒蘸取滤液点于pH试纸上待颜色变化稳定后用标准比色卡比对得出pH数值 盐酸 防止局部温度过高,导致液滴飞溅
A a 漏斗 用玻璃棒蘸取滤液点于pH试纸上待颜色变化稳定后用标准比色卡比对得出pH数值 盐酸 防止局部温度过高,导致液滴飞溅
【解析】
(1)某同学打算用高锰酸钾制取并收集干燥的气体,则可选择固体加热装置B;氧气的密度大于空气,应该用向上排空气法收集,选择装置D;高锰酸钾加热产生锰酸钾、二氧化锰和氧气的化学方程式![]() 。
。
(2)若打算制取二氧化碳,则应选择固液发生装置(不需要加热)A,在C装置中装入浓硫酸来干燥制取的气体,则应该“长管进、短管出”从a端通入气体进行干燥。
(3)①对固体残留物进行过滤,除了需要玻璃棒和烧杯外,还需要的玻璃仪器是漏斗(带滤纸,用于过滤);
②用pH试纸检测滤液的酸碱度,检测pH的操作方法是:把一片pH试纸置于干燥洁净的表面皿上,用玻璃棒蘸取滤液点于pH试纸上待颜色变化稳定后用标准比色卡比对得出pH数值;测得溶液pH=4,说明混合溶液显酸性,有盐酸剩余。
③取上述少量滤液进行蒸发,蒸发过程玻璃棒不断搅拌的作用是:防止局部温度过高,导致液滴飞溅。


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:
【题目】某兴趣小组开展“测定密闭容器中某种气体的体积分数”的探究实验。
(实验1)按图1所示装置,用红磷燃烧的方法测定空气中氧气的体积分数。
(实验2)按图2所示装置,在集气瓶内壁用水均匀涂附铁粉除氧剂(其中辅助成分不干扰实验),利用铁锈蚀原理测定空气中氧气的体积分数。
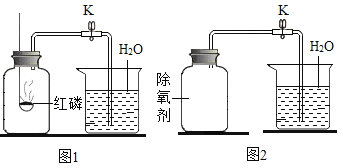
(1)实验1中,红磷燃烧的主要现象是_______。红磷燃烧的化学方程式是____,红磷熄灭后,集气瓶冷却至室温,打开K,水能倒吸入集气瓶的原因是___。
(2)为提高实验的准确性,以上两个实验都需要注意的事项是______(写一点)。
(3)实验过程中,连接数字传感器,测得实验1、实验2中氧气的体积分数随时间变化的关系分别如图3、图4所示。依据图3、图4信息,_________(填“实验1”或“实验2”)的测定方法更准确,判断依据是_________。
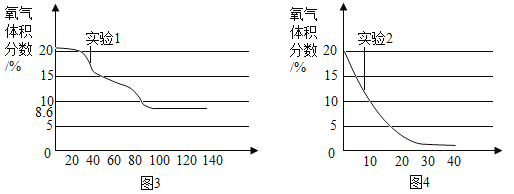
(4)结合你的学习经验,若要寻找红磷或铁粉除氧剂的替代物,用图1或图2装置测定空气中氧气的体积分数,该替代物应满足的条件是_________(写两点)。
(实验3)测定用排空气法收集到的集气瓶中二氧化碳的体积分数。
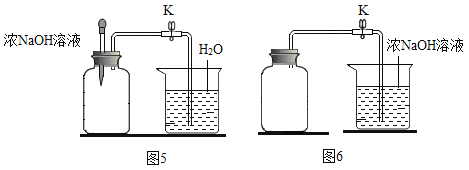
(5)甲同学设计图5所示装置进行测定。浓NaOH溶液的作用是 ____(用化学方程式表示)。
(6)乙同学提出,仅利用图6所示装置,在不添加其他试剂的前提下,也能测得集气瓶中二氧化碳的体积分数。为达到实验目的,操作方法是___________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学是从微观角度研究物质性质、组成、结构及其变化规律的科学,根据图示填空:
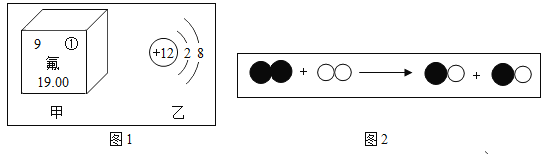
(1)图1甲中,①代表的元素符号是__,其原子的结构示意图为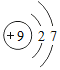 ,则由甲、乙元素组成化合物氟化镁的化学式为__.
,则由甲、乙元素组成化合物氟化镁的化学式为__.
(2)氢气、金刚石、硫酸铜三种物质中由离子构成的物质是__(填化学式).
(3)元素周期表中不同元素间最本质的区别是__(填字母).
A 电子数不同 B 中子数不同 C 相对原子质量不同 D 质子数不同
(4)图2为某化学反应的微观示意图.该反应的前后总共有__种分子,反应前后各元素的化合价__(填“有”或“无”)变化.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图是甲乙两种固体物质的溶解度曲线。据图回答:[来源
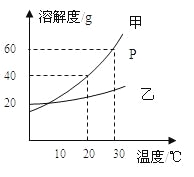
(1)P点的含义是__________________________。
(2)20℃时要使接近饱和的甲溶液变成饱和溶液,可采用的方法有 _________(写出一种)
(3)当甲中含有少量乙时,可采用____________的方法提纯甲 。
(4)30℃时,将40g甲物质放入盛有50g水的烧杯中,所得溶液溶质的质量分数为______;若将烧杯内物质升温到50℃(不考虑水蒸发),溶液中变化的是_____(选填A、B、C、D)
A、溶剂的质量 B、溶液的质量C、溶质的质量分数D、以上都不变
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】a,b两种物质的溶解度曲线如下图所示.下列说法不正确的是
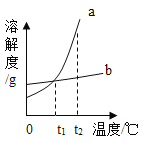
A.将![]() ℃时b的饱和溶液加水可变为不饱和溶液
℃时b的饱和溶液加水可变为不饱和溶液
B.将![]() ℃时a的饱和溶液降温至
℃时a的饱和溶液降温至![]() ℃,溶液质量不变
℃,溶液质量不变
C.![]() ℃时,两种物质的饱和溶液中溶质质量分数a
℃时,两种物质的饱和溶液中溶质质量分数a![]() b
b
D.将![]() ℃时a、b的饱和溶液分别降温至
℃时a、b的饱和溶液分别降温至![]() ℃,两溶液的溶质质量分数相等
℃,两溶液的溶质质量分数相等
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列实验方案不能达到实验目的是( )
序号 | A | B | C | D |
目的 | 证明二氧化碳溶于水且能和水反应 | 证明碳与氧化铜能发生反应 | 探究同种溶质在不同的溶剂的溶解性 | 探究燃烧的条件是燃烧需要氧气 |
方案 |
|
|
|
|
A. AB. BC. CD. D
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】废铁屑主要成分是铁,还有少量铁锈(Fe2O3),硫酸亚铁的生产工艺如图所示。

(1)在反应器中除发生Fe2O3+3H2SO4=Fe2(SO4)3+3H2O,Fe2(SO4)3+Fe═3FeSO4这两个反应外,还会发生另外一个反应,化学方程式为:_____,反应器要加强通风,严禁烟火,其原因是:_____。
(2)将成品在有氧条件下焙烧,可转化为Fe2O3、SO2和SO3.为了提高SO3的产率,某实验小组进行了系列探究,实验数据如下:
编号 | 空气通入量/Ls﹣1 | 温度/℃ | SO2产率% | SO3产率/% |
a | 0.02 | 850 | 45.4 | 54.6 |
b | 0.06 | 850 | 30.5 | 69.5 |
c | 0.10 | 810 | 11.1 | 88.9 |
d | 0.10 | 850 | 11.1 | 88.9 |
e | 0.10 | 890 | 11.2 | 88.8 |
①本实验主要研究了哪些因素对SO3产率的影响_____。
②根据上表数据,生产过程中采用实验_____(填编号)的提取条件最合理。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】将氯化钠和氯化铜的固体混合物20g完全溶于100g水中,再向所得的溶液中加入溶质质量分数为10%的NaOH溶液。有关的变化如图所示。(反应的化学方程式为:CuCl2+2NaOH=Cu(OH)2↓+2NaCl)请计算:
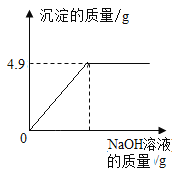
(1)NaOH中氧元素和氢元素的质量比为______________。
(2)求恰好完全反应时,所用NaOH溶液的质量。(写出计算过程)
(3)求恰好完全反应时溶液中溶质的质量分数。(写出计算过程,结果精确到0.1%)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图是某反应的微观示意图(其中“![]() ”和“
”和“![]() ”分别表示不同的原子)。
”分别表示不同的原子)。
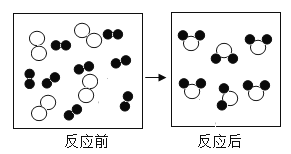
(1)该反应有_______种生成物
(2)反应后方框内应再填入___个“![]() ”微粒。
”微粒。
(3)参加反应的“![]() ”和“
”和“![]() ”分子的个数比是_______。
”分子的个数比是_______。
(4)请从微观的角度分析化学变化的实质是___。
(5)上述反应中,一定不改变的是_____(填字母序号)。
A 元素种类
B 分子种类
C 原子种类
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com