

分析 酒精灯是常用的加热仪器,集气瓶是收集气体的仪器;制取装置包括加热和不需加热两种,如果用双氧水和二氧化锰制氧气就不需要加热,如果用高锰酸钾或氯酸钾制氧气就需要加热.氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集.实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热.二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集;二氧化碳的验满方法是:将一根燃着的木条平放在集气瓶口,木条熄灭,证明满了.有关的计算要准确.
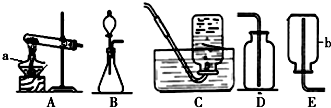
解答 解:(1)酒精灯是常用的加热仪器,集气瓶是收集气体的仪器,故答案为:酒精灯;集气瓶
(2)如果用高锰酸钾制氧气就需要加热,氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集,故答案为:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;A;C 或 D;
(3)实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热,二氧化碳的验满方法是:将一根燃着的木条平放在集气瓶口,木条熄灭,证明满了;故答案为:CaCO3+2HCl=CaCl2+H2O+CO2↑; 木条火焰熄灭.
(4)虽然常温常压下乙烯(C2H4)不与空气反应,但因密度很接近空气而不用排空气法收集.若用排空气法收集乙烯,结果是不易排尽瓶内空气,导致收集到的气体不纯;排水法收集乙烯时,待导气管口连续稳定地冒出气泡才开始收集,原因是以免收集到的气体因混有空气而不纯;
(5)①用下列方案收集“$\frac{1}{2}$集气瓶的氧气”,其中最合理的是排水法;
②用排水法收集气体时,如果观察到集气瓶口旁有气泡逸出,则集气瓶中气体已收集满.
③可设一瓶气体的体积为1L,因为空气中氧气的体积分数约为21%,则实验中,集气瓶内的氧气约占总体积的体积分数是:$\frac{21%×\frac{1}{2}L+\frac{1}{2}L}{1L}$×100%=60.5%
故答案为:①a;②观察到集气瓶口旁有气泡逸出;③60.5.
故答案为:
(1)酒精灯; 集气瓶.
(2)2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑,分解反应,A,C或D.
(3)CaCO3+2HCl=CaCl2+H2O+CO2↑;木条火焰熄灭.
(4)不易排尽瓶内空气,导致收集到的气体不纯;以免收集到的气体因混有空气而不纯.
(5)①a.②观察到集气瓶口旁有气泡逸出.③60.5.
点评 本考点主要考查了仪器的名称、气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写和有关的计算等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.


 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案科目:初中化学 来源: 题型:选择题
| A. | ③⑤ | B. | ④⑤ | C. | ①③ | D. | ⑤ |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | O→+2 | B. | +2→O | C. | +4→O | D. | +4→+2 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 时间(min) 浓度 催化剂 | 30%H2O2溶液 | 15%H2O2溶液 | 5%H2O2溶液 |
| 加入W g MnO2 | 0.2 | 0.8 | 2.0 |
| 加入W g Fe2O3 | 7.0 | 9.0 | 16.0 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com