

分析 (1)根据实验室中制取二氧化碳的反应原理和反应条件来选择反应的发生装置,根据二氧化碳的密度及水溶性来选择收集装置.
(2)A装置属于固体加热型,进行分析解答.
解答 解:(1)实验室中制取二氧化碳常用大理石或石灰石和稀盐酸反应来制取,属于固液常温型,所以应该选择B装置来制取二氧化碳气体;二氧化碳密度比空气大,能溶于水,应用向上排空气法收集,所以应该选择C装置来收集二氧化碳.
(2)实验室制氧气的发生装置可以选用A装置,A装置属于固体加热型,选择A装置的依据是反应物是固体,反应条件是加热.
故答案为:(1)BC;(2)反应物是固体,反应条件是加热.
点评 本题难度不大,是中考的重要考点之一,熟练掌握实验室中制取气体的反应原理、发生装置和收集装置的选择依据等是正确解答本题的关键.


 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案科目:初中化学 来源: 题型:填空题
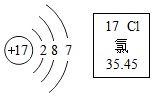
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 2017年4月长春应用化学研究所提出了一种独特的锂-氮电池(LI-N2),结构示意图见左图,该电池由锂箔作负极,多孔碳布作正极,玻璃纤维作隔板,可以直接利用空气中的氮气,锂-氮电池的反应方程式:6Li+N2=2Li3N.请回答:
2017年4月长春应用化学研究所提出了一种独特的锂-氮电池(LI-N2),结构示意图见左图,该电池由锂箔作负极,多孔碳布作正极,玻璃纤维作隔板,可以直接利用空气中的氮气,锂-氮电池的反应方程式:6Li+N2=2Li3N.请回答:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 碳酸盐与酸反应会放出气体,能与酸反应放出气体的物质不一定是碳酸盐 | |
| B. | 中和反应一定有盐和水生成,生成盐和水的反应一定是中和反应 | |
| C. | 二氧化碳能使燃着的木条熄灭,能使燃着木条熄灭的气体一定是二氧化碳 | |
| D. | 单质是由同种元素组成的,由同种元素组成的物质一定是单质 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 根据如图中甲、乙、丙三种固体物质的溶解度曲线,回答下列问题.
根据如图中甲、乙、丙三种固体物质的溶解度曲线,回答下列问题.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 序号 | 错误实例 | 错误分析 |
| A | 铁与稀硫酸生成硫酸铁 | 反应产物不正确 |
| B | FeCl3+3NaOH═Fe(OH)3+NaCl | 只缺少沉淀符号 |
| C | 2KMnO4═K2MnO4+MnO2+O2↑ | 反应条件不正确 |
| D | 氢氧化钠俗名烧碱或纯碱 | 俗名中的纯碱不正确 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

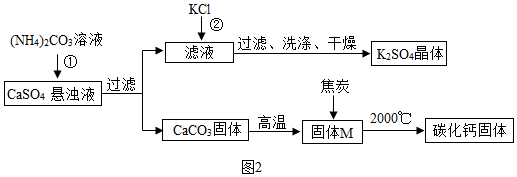

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com