
| 第一次 | 第二次 | 第三次 | |
| O2的质量(g) | 3 | 4 | 6 |
| P2O5的质量(g) | 5.33 | 7.1 | 7.1 |
分析 (1)根据化学方程式表示的意义解答,化学方程式中各物质的质量比等于物质的相对分子质量乘以化学式前面的系数之比.
(2)先根据磷在氧气中燃烧这一反应中各物质间的质量比算出在3克氧气中燃烧了的磷的质量,再根据质量守恒定律,生成五氧化二磷的质量,即可最结果做出判断;
(3)根据磷在氧气中燃烧这一反应中各物质间的质量比可以算出在4克氧气中燃烧了的磷的质量,再根据质量守恒定律,生成五氧化二磷的质量,即可求出第二次生成五氧化二磷的质量;根据同样的方法即可确定第三次生成五氧化二磷的质量.
解答 解:(1)在4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5中,P、O2、P2O5的质量比=(31×4):(32×5):(142×2)=124:160:284.
(2)根据磷在氧气中燃烧这一反应中各物质间的质量比可以得出:124:160=x:3g,由此可以算出在3克氧气中燃烧了的磷的质量为2.33g,由于氧气不足,3.1g磷无法完全燃烧,根据质量守恒定律,生成五氧化二磷的质量为:3g+2.33g=5.33g,故第一次不能生成6.1克五氧化二磷.
(3)根据磷在氧气中燃烧这一反应中各物质间的质量比可以得出:124:160=x:4g,由此可以算出在4克氧气中燃烧了的磷的质量为3.1g,也就是说3.1g磷与4g氧气恰好完全反应,根据质量守恒定律,生成五氧化二磷的质量为:3.1g+4g=7.1g,故第二次生成7.1克五氧化二磷;在第三次实验中氧气的质量增加为6g后,由于磷的质量没有增加,生成五氧化二磷的质量也不会增加了,仍为7.1g.
故答案为:(1)124:160:284;(2)氧气不够;(3)7.1;7.1.
点评 本题主要考查学生运用化学方程式和质量守恒定律综合分析和解决实际问题的能力.增加了学生分析问题的思维跨度,强调了学生整合知识的能力.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:推断题
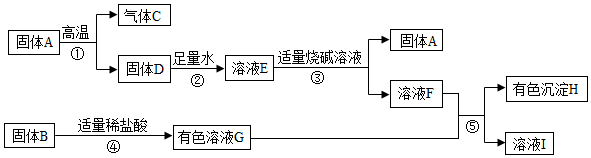
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 13克 | B. | 67克 | C. | 31克 | D. | 23克 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
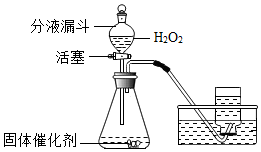 实验室里还可采用如图装置,通过分解过氧化氢(H2O2)的方法制取氧气.
实验室里还可采用如图装置,通过分解过氧化氢(H2O2)的方法制取氧气.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 物质 | 操作 | |
| A | 纯水和矿泉水 | 蒸发,观察是否有固体残留物 |
| B | 水和双氧水 | 加入少量二氧化锰,观察现象 |
| C | 二氧化碳、氧气和氮气 | 将燃着的木条分别伸入瓶中,观察现象 |
| D | 活性炭和氧化铜 | 分别投入盛有红棕色二氧化氮气体的集气瓶中,观察现象 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
 ”和“
”和“ ”分别表示两种不同元素的原子:
”分别表示两种不同元素的原子:
 ”聚集成的物质可能(填“可能”或“不可能”)是氧化物,参加反应的两种反应物“
”聚集成的物质可能(填“可能”或“不可能”)是氧化物,参加反应的两种反应物“ ”与“
”与“ ”的分子个数比为2:1,此反应的基本反应类型为化合反应;若由“
”的分子个数比为2:1,此反应的基本反应类型为化合反应;若由“ ”和“
”和“ ”构成的物质的相对分子质量分别为28、32,则由“
”构成的物质的相对分子质量分别为28、32,则由“ ”构成的物质的相对分子质量为44.
”构成的物质的相对分子质量为44.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com