
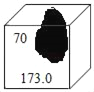
【题目】某元素在元素周期表中的一格如图所示,其中部分受损。
(1)请你推测该元素属于_____(填“金属”或“非金属”)元素;
(2)该元素的原子其核内中子数为_____,核外电子数为_____。
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:
【题目】小林同学在体育课上腿部擦伤,医务室的大夫在她伤口上涂了医用过氧化氢溶液,小林看到伤口处产生了小气泡,很好奇。为什么瓶中的过氧化氢溶液涂到伤口上,分解就加快了呢?

I.小林准备用如下图所示装置测定过氧化氢分解的快慢,实验前在注射器中吸入过氧化氢溶液,量筒内装满水。实验开始时,向试管中注入过氧化氢溶液,并用排水法收集氧气。记录2分钟收集的气体体积。
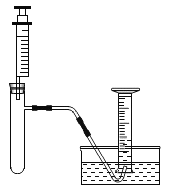
(1)请写出过氧化氢分解的反应方程式:______________。
(2)若要检验生成的气体是否为氧气,可将导气管从水中取出,取带火星的木条放在导气管口处,观察到__________,说明生成的气体是氧气。
II.小林查阅了相关资料,并进行了探究实验
(查阅资料)
(1)过氧化氢是人体代谢废物之一,它能够对机体造成损害,人体存在过氧化氢酶,可以催化过氧化氢分解。
(2)温度对化学反应的快慢有影响,人体正常体温是37℃。
(提出猜想)猜想1: 过氧化氢分解加快是因为体温比瓶中的温度高。
猜想2:过氧化氢分解加快是因为伤口中有过氧化氢酶。
(进行实验)
序号 | 实验步骤 | 实验现象 | 实验结论 |
① | 分两次进行实验,均注入5 mL过氧化氢溶液 第一次在常温下进行 第二次将试管浸在37℃的温水中 | 量筒中2分钟收集到的气体体积均为5 mL | _____ |
② | 分两次进行实验 第一次将装有一小粒过氧化氢酶的试管浸在37℃的温水中,注入5 mL过氧化氢溶液 第二次__________ | 第一次,量筒中2分钟收集到的气体体积为56 mL 第二次,量筒中2分钟收集到的气体体积为5 mL | 过氧化氢分解加快是因为过氧化氢酶的作用 |
(3)实验①得出的结论是___________。
(4)实验②中第一次收集到的氧气体积为__________ mL。
(5)实验②中横线部分应进行的操作是__________。
(实验反思)
小林反思了实验过程,认为人体中过氧化氢酶是在体温条件下发挥作用的,实验得出的结论可能存在不足。因此又补充进行了几组实验,数据记录如下表所示。
加入过氧化氢酶 | 不加过氧化氢酶 | |||||
反应温度/ ℃ | 25 | 37 | 42 | 25 | 37 | 42 |
收集到气体体积/ mL | 39 | 56 | 34 | 5 | 5 | 5 |
(6)通过这些数据,你能得出的新结论是__________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是几种粒子的结构示意图:

(1)A~E共有_____种元素,B所表示的元素位于元素周期的第____周期,该元素的原子容易 ______(填“得到”或“失去”)电子。
(2)表示阳离子的有_________(填离子符号);表示阴离子的有 _________(填离子符号);
(3)表示原子的粒子有________(填序号);表示相对稳定结构的有 ________(填序号);
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图是“尾气催化转换器”将汽车尾气中有毒气体转变为无毒气体的微观示意图,其中不同的圆球代表不同原子。下列说法错误的是
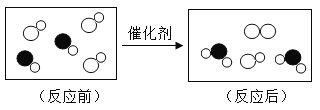
A. 此反应有单质生成
B. 原子在化学变化中是不可分的
C. 图中生成物全部是化合物
D. 参加反应的两种分子的个数比为1∶1
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图是配制溶质质量分数为10%的NaCl溶液的实验操作示意图:
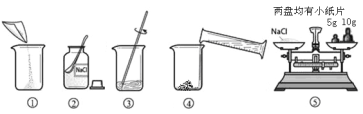
(1)用上图表示的序号表示配制溶液的正确操作顺序__________;
(2)图③中,使用玻璃棒搅拌的作用是___________;
(3)称量NaCl时,天平平衡后的状态如图⑤所示,游码标尺示数见图,则称取的NaCl质量为______;
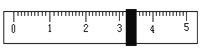
(4)称量NaCl完毕放回砝码时,发现有一个砝码缺损了一个小角,若其他操作步骤正确,则所配溶液的溶质质量分数_____(填“大于”、“小于”或“等于”)10%。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是酒石酸的分子结构,酒石酸是一种酸﹐存在于多种植物中﹐如葡萄中就含有酒石酸。它可以作为食品中添加的抗氧化剂﹐以使食物具有酸味,是发酵粉的成分之一。下列关于酒石酸的说法中正确的是( )

A. 酒石酸是由碳、氢、氧三种原子构成的化合物
B. 酒石酸分子中氧元素的质量分数最大
C. 酒石酸分子中质子数与中子数之比为1:1
D. 酒石酸的化学式是C4H6O6,溶于水能与碳酸钠反应生成CO2
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】鸡蛋壳的主要成分是碳酸钙(其它成分不溶于水也不与酸反应)。化学兴趣小组为了测定鸡蛋壳中碳酸钙的含量,做如下实验。反应①结束后,所加盐酸刚好反应了一半,反应②恰好完全反应。

请回答下列问题:
(1)反应①的化学方程式为________;
(2)根据已知条件列出求解碳酸钙质量(X)的比例式______________;
(3)该鸡蛋壳中碳酸钙的质量分数为_______;
(4)溶液b中溶质的质量分数为_______;
(5)用36.5%的浓盐酸配制80g上述稀盐酸需加水的质量为_______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】图1是两种元素在元素周期表中的信息,图2是氟原子的原子结构示意图。
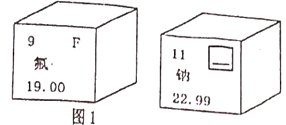
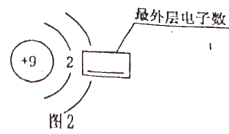
(1)图1方框的横线上填的是_____________;图2方框横线上的数字是________。
(2)钠元素属于_____________(填“金属”或“非金属”)元素;图1所示两种元素形成化合物的化学式为_____________。此物质由_____________(填分子、原子或离子)构成。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是甲、乙两种物质的溶解度曲线。下列有关叙述正确的是( )
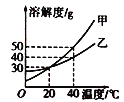
A. 20℃时,100g甲、乙两种物质的溶液中含有相同质量的溶质
B. 甲、乙的饱和溶液从40℃降温到20℃,析出固体质量甲>乙
C. 乙中混有少量甲时,可采用冷却热饱和溶液结晶的方法提纯甲
D. 将100g溶质质量分数为20%的甲溶液从40℃降温至20℃,其溶质的质量分数仍然为20%
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com