
【题目】如图所示装置可用于实验室制取某些气体,并能随开随用。下表中所选用的药品及制取的气体完全正确的一组是( )
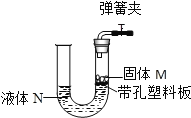
选项 | 选用药品 | 制取的气体 | |
固体M | 液体N | ||
A | 锌粒 | 稀硫酸 | 氢气 |
B | 碳酸钠 | 浓盐酸 | 二氧化碳 |
C | 大理石 | 稀盐酸 | 二氧化碳 |
D | 二氧化锰 | 过氧化氢 | 氧气 |
A.AB.BC.CD.D
科目:初中化学 来源: 题型:
【题目】为了测定蜡烛中碳、氢两种元素的质量比,某化学兴趣小组设计了如下图所示的实验装置,实验步骤如下:先分别称量蜡烛、装置Ⅱ、装置Ⅲ的质量。按图示连接好仪器,点燃蜡烛,同时从a导管口抽气,一段时间后熄灭蜡烛,再分别称量蜡烛、装置Ⅱ、装置Ⅲ的质量,实验数据如下表所示:(浓硫酸有吸水性,氢氧化钠和氧化钙既可吸水,又可吸收二氧化碳)
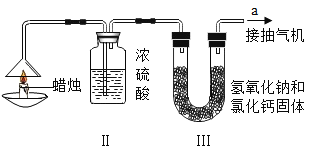
蜡烛 | 装置Ⅱ | 装置Ⅲ | |
反应前的质量/g | 15.8 | 182.3 | 212.2 |
反应后的质量/g | 14.4 | 184.1 | 216.6 |
(1)该实验中测得水的质量为_______g,二氧化碳的质量为_______g。
(2)由该实验数据计算,蜡烛中碳、氢元素的质量之比为_______。
(3)装置Ⅱ和装置Ⅲ的顺序能否颠倒?_______(填“能”或“不能”)。
(4)理论上,装置Ⅱ和装置Ⅲ增加的总质量大于蜡烛减小的质量,其原因是_______。
(5)该实验能否准确测出蜡烛燃烧生成二氧化碳和水的质量?____(填“能”或“不能”),理由是____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某化学小组同学从微观角度进一步理解复分解反应的实质.
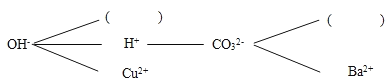
(1)复分解反应的实质是某些阴、阳离子结合生成沉淀、气体或____的过程.
(2)根据复分解反应的实质,形成一个复分解反应网络图(如图所示,图中直线相连的阴、阳离子之间能够两两结合发生反应),请选择合适的离子填入如图括号内(________)、(________),使其两两结合时,一个有气体产生,一个有沉淀(注:沉淀与珍珠粉的成分相同)生成,其中有气体生成的化学反应方程式可能是_______________.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】乳酸亚铁片可用于治疗缺铁性贫血。下图为乳酸亚铁片说明书上的部分文字。请仔细阅读后回答以下问题:

(1)1个乳酸亚铁分子中有______原子。
(2)117g乳酸亚铁中铁元素的质量为____g。
(3)某人每天分二次服药,一次最多服用____片,服药时不能喝茶的原因是______ 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】镁是叶绿素中唯一的金属元素。植物缺镁时,通常的症状表现为叶片失绿,严重时整片叶干枯。给农作物施加MgSO4和NH4MgPO4(磷酸镁铵)等镁肥,可以促进光合作用,提高抗病能力。
(1)NH4MgPO4中含有________种元素,其相对分子质量是________________。
(2)NH4MgPO4中Mg元素的质量分数是________________(精确到0.1%)。
(3)现要配制溶质量分数为2%的MgSO4溶液500kg进行喷施,需25% MgSO4溶液的质量是___________kg。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某兴趣小组在相同条件下,将10.00g下列物质分别置于相同规格的烧杯,并敞口存放于空气中,烧杯中物质质量随时间变化如下表,回答下列问题。
时间 | 质量/g | |||||
水 | 饱和石灰水 | 稀盐酸 | 浓硫酸 | 氢氧化钠浓溶液 | 氯化钙溶液 | |
1天 | 8.16 | 8.37 | 8.64 | 11.18 | 9.38 | 10.25 |
2天 | 5.76 | 5.94 | 6.69 | 12.55 | 8.47 | 10.33 |
(1)下列图示能反映水在空气中放置时发生变化的微观示意图是_________(填字母序号)。图中表示氧原子,表示氢原子)

(2)石灰水在空气中久置后有浑浊现象,写出该反应的化学方程式___________________。
(3)为研制一种安全、环保的除湿剂,可选择上表中的__________________(填溶质的化学式)。
(4)将10.00g氯化钠浓溶液敞口久置后,最终得到2.26g晶体,则该溶液是________(填“饱和”或“不饱和”)溶液。(已知该温度下氯化钠溶解度为36.1g)
(5)为进一步研究稀盐酸敞口久置后浓度变化,该小组开展如下探究。
①甲同学猜想浓度可能会变大,理由是_______________________。
②为验证甲同学的猜想是否正确,设计实验方案:_________________________。
(注意:若答对第(6)小题奖励4分,化学试卷总分不超过60分。)
(3)乙同学取20%的氢氧化钠溶液20.00g,敞口放置一段时间后部分变质,得到18.80g溶液,由此能否计算所得溶液中溶质组成?若能,请计算其组成;若不能,请补充完成实验方案设计,同时说明需要测定的数据(用a表示),并计算a的取值范围___________。(不要求写出计算过程)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】2019年底,徐宿淮盐铁路将建成通车,淮安人可实现高铁出行。
(1)高铁在建造时使用了大量的新材料,下列属于金属材料的是______(填序号)。

A 生产高铁车头的玻璃钢
B 制造高铁车身的镁铝合金
C 制造轨道枕木的聚氨酯材料
D 建筑高铁路基的钢筋混凝土
(2)高铁刹车制动盘使用合金锻钢制作,主要利用该合金耐高温、______等特性。
(3)在高铁站的建设中,使用了大量的钢铁。工业上用赤铁矿(主要成分是氧化铁)和一氧化碳反应冶炼铁,该反应的化学方程式为______。
(4)高铁轨道焊接时,可用铝热反应:2Al+Fe2O3![]() 2Fe+Al2O3,该反应的基本类型是______。
2Fe+Al2O3,该反应的基本类型是______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】氯是一种重要的“成盐元素”,在海水、盐湖和盐矿中广泛存在。
(1)卤水点豆腐时常用到氯化镁,氯化镁的化学式为_____。
(2)构成氯化钙的基本微粒是离子,则钙离子的化学符号为_____,氯原子的结构示意图为_____。
(3)次氯酸钠(NaClO)溶液吸收SO2的化学方程式为:NaClO+SO2+H2O=NaCl+X,则X的化学式为_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】为除去粗盐中含有的硫酸钠、氯化镁、氯化钙等杂质,应加入过量的氯化钡、氢氧化钠、碳酸钠等物质将杂质转化为沉淀过滤除去,再向滤液中加入适量的盐酸得到精盐水。该过程示意如图:
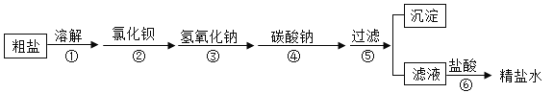
对该过程的认识中,正确的是( )
A.①操作中需要进行搅拌,目的是提高氯化钠的溶解度
B.②、④两步操作顺序可以颠倒
C.⑤操作得的沉淀中共有三种物质
D.⑥操作中,加入盐酸的目的是除去过量的氢氧化钠和碳酸钠,将滤液的pH调为7
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com