
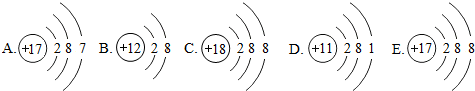
分析 (1)元素是质子数(即核电荷数)相同的一类原子的总称,决定元素种类的是质子数(即核电荷数),进行分析解答.
(2)若粒子的最外层电子数为8(氦为2个),属于相对稳定结构.
(3)当质子数<核外电子数,为阴离子.
解答 解:(1)根据不同种元素最本质的区别是质子数不同,A和E核内质子数相同,属于同一种元素,图中共表示4种元素.
(2)BCE的最外层为电子数均为8,均属于相对稳定结构.
(3)E、质子数=17,核外电子数=18,质子数<核外电子数,为带1个单位负电荷的阴离子,其离子符号为:Cl-.
故答案为:(1)4;(2)BCE;(3)Cl-.
点评 本题难度不大,考查学生对粒子结构示意图及其意义的理解,明确粒子中核内质子数和核外电子数之间的关系是解题的关键.


科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
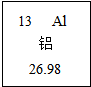
| A. | 铝元素属于金属元素 | B. | 铝元素的原子序数为13 | ||
| C. | 铝元素的相对原子质量为26.98 | D. | 铝元素位于元素周期表中第三周期 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
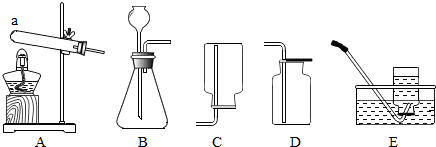
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 滤纸上有Ag,滤液中有Ag+、Cu2+、Zn2+、Fe2+ | |
| B. | 滤纸上有Ag、Cu,滤液中有Ag+、Zn2+、Fe2+ | |
| C. | 滤纸上有Ag、Cu、滤液中有Zn2+、Cu2+Fe2+ | |
| D. | 滤纸上有Ag、Cu、Fe、滤液中有Zn2+、Fe2+ |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
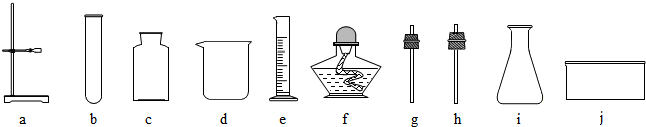
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com