
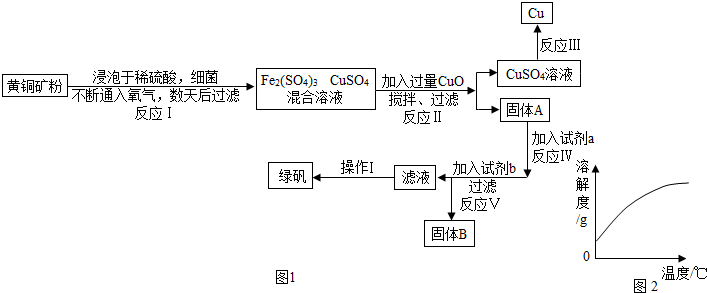
分析 (1)根据加入过量的氧化铜调节pH值,使铁离子变成氢氧化铁沉淀进行分析;
(2)根据铁和硫酸铜反应生成硫酸亚铁和铜进行分析;
(3)根据固体A的成分是氧化铜和氢氧化铁,酸会与金属氧化物和不溶性碱反应,所以a是稀硫酸进行分析;
(4)根据铁会与硫酸铁反应生成硫酸亚铁,铁会与硫酸铜反应生成硫酸亚铁和铜进行分析;
(5)根据硫酸亚铁的溶解度曲线进行分析.
解答 解:(1)加入过量的氧化铜调节pH值,使铁离子变成氢氧化铁沉淀,所以固体A的成分的化学式是:CuO、Fe(OH)3;
(2)铁和硫酸铜反应生成硫酸亚铁和铜,化学方程式为:Fe+CuSO4=FeSO4+Cu;
(3)固体A的成分是氧化铜和氢氧化铁,酸会与金属氧化物和不溶性碱反应,所以a是稀硫酸,控制加入的a试剂适量的方法是:固体完全消失,停止加稀硫酸;
(4)铁会与硫酸铁反应生成硫酸亚铁,铁会与硫酸铜反应生成硫酸亚铁和铜,所以试剂b为铁,且要过量的目的是使硫酸铜、硫酸铁完全转化成硫酸亚铁;
(5)通过分析溶解度曲线可知,欲从溶液中获得绿矾晶体,分离操作Ⅰ应为蒸发浓缩、降温结晶、过滤,用少量冰水洗涤绿矾固体2-3次.
故答案为:(1)CuO、Fe(OH)3;
(2)Fe+CuSO4=FeSO4+Cu;
(3)稀硫酸,固体完全消失,停止加稀硫酸;
(4)铁,使硫酸铜、硫酸铁完全转化成硫酸亚铁;
(5)降温结晶,冰水.
点评 在解此类题时,首先分析题中考查的问题,然后结合学过的知识和题中的提示进行解答.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:选择题
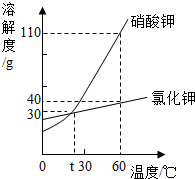 如图是硝酸钾和氣化钾的溶解度曲线,下列说法正确的是( )
如图是硝酸钾和氣化钾的溶解度曲线,下列说法正确的是( )| A. | 硝酸钾的溶解度一定大于氯化钾的溶解度 | |
| B. | t℃时,硝酸钾溶液的浓度一定等于氯化钾溶液的浓度 | |
| C. | 把60℃时硝酸钾溶液降温至30℃,一定有硝酸钾晶体析出 | |
| D. | 60℃时,把50 g上述物质分别加入到50 g水中,充分溶解得到硝酸钾溶液的质量一定大于氯化钾溶液的质量 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
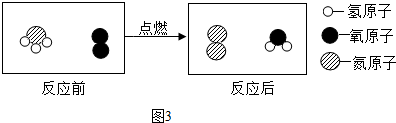
 ”表示一个氢原子,则“
”表示一个氢原子,则“ ”表示H2(填化学符号)
”表示H2(填化学符号)查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 油脂属于高分子化合物 | |
| B. | 豆油、猪油、汽油都属于油脂 | |
| C. | 加碘食盐遇到淀粉水溶液后会变蓝 | |
| D. | 谷物、甘薯在酿酒过程中,淀粉不能直接转化为乙醇 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 液体名称 | 白醋 | 蒸馏水 | 食盐溶液 | 肥皂水 | 碱溶液 |
| 紫甘蓝汁液显示的颜色 | 红色 | 蓝紫色 | 蓝紫色 | 蓝色 | 绿色 |
| PH | 7~9 | 10~11 | 12~14 |
| 紫甘蓝汁液显示的颜色 | 蓝色 | 绿色 | 黄色 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
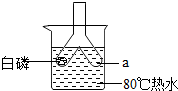 用如图所示装置研究可燃物燃烧的条件.
用如图所示装置研究可燃物燃烧的条件.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com