
| A. | 硬水和软水-观察颜色 | |
| B. | 氯化钾和氯化铵-氢氧化钠 | |
| C. | 合成纤维和羊毛纤维-点燃闻气味 | |
| D. | 一氧化碳和二氧化碳-灼热的氧化铜 |
分析 A、根据硬水和软水都是透明澄清的解答;
B、根据铵态氮肥和碱混合会生成氨气进行分析;
C、根据合成纤维和羊毛纤维的成分及蛋白质的鉴别方法分析;
D、根据一氧化碳和二氧化碳的性质方面进行分析、判断.
解答 解:
A、硬水和软水都是透明澄清的,所以不能通过观察是否澄清、透明进行区分,故错误;
B、取样品,加入氢氧化钠研磨,有刺激性气味的气体产生的是氯化铵,没有明显现象的是氯化钾,现象不同,可以鉴别,故正确;
C、羊毛是天然纤维,含有蛋白质,涤纶是合成纤维,羊毛点燃会有烧焦羽毛的气味,而涤纶只会缩成一团,现象不同,可以鉴别,故正确;
D、一氧化碳能使灼热的氧化铜变成红色,二氧化碳不能使灼热的氧化铜变成红色.故正确.
答案:A
点评 在解此类题时,首先分析被鉴别物质的性质,然后选择适当的试剂和方法,出现不同的现象即可鉴别.


 名校课堂系列答案
名校课堂系列答案科目:初中化学 来源: 题型:选择题
| A. | 电解水实验中,与电源负极相连的电极上产生的气体是氢气 | |
| B. | 细铁丝在氧气中燃烧,火星四射,生成红色固体 | |
| C. | 硫在氧气中燃烧,发出蓝紫色火焰,生成有刺激性气味的气体 | |
| D. | 红磷在空气中燃烧产生大量白雾 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 铝的金属活动性比铁强,则铝制品比铁制品更容易锈蚀 | |
| B. | 水和过氧化氢的组成元素相同,则两者的化学性质相同 | |
| C. | 化合物是由不同种元素组成的纯净物,则只含有一种元素的物质一定不是化合物 | |
| D. | 碳酸盐遇酸有气体产生,则与酸反应产生气体的一定是碳酸盐 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

| 可能的原因 | 实验步骤 | 实验现象 | 实验结论 |
| 原因一: | 猜想的结论正确 | ||
| 原因二: |
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
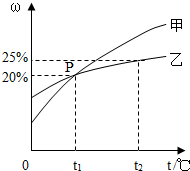 甲和乙两种固态物质的饱和溶液中溶质质量分数(ω)与温度(T)的关系如图所示.
甲和乙两种固态物质的饱和溶液中溶质质量分数(ω)与温度(T)的关系如图所示.查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 实验编号 | 钠块大小 | 硫酸铜溶液 | 实验中产生沉淀的现象 |
| ① | 绿豆大小 | 稀溶液10ml | 产生蓝绿色沉淀 |
| ② | 绿豆大小 | 浓溶液10ml | 产生蓝色絮状沉淀 |
| ③ | 豌豆大小 | 稀溶液10ml | 产生蓝色絮状沉淀 |
| ④ | 豌豆大小 | 浓溶液10ml | 产生蓝色絮状沉淀,并出现黑色固体 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
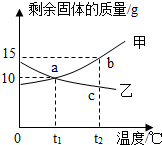 将质量均为30g的甲、乙两种固体分别加入到50g水中,充分搅拌后,剩余固体物质与温度的关系如图所示,下列说法正确的是( )
将质量均为30g的甲、乙两种固体分别加入到50g水中,充分搅拌后,剩余固体物质与温度的关系如图所示,下列说法正确的是( )| A. | 甲的溶解度随温度升高而增大 | |
| B. | t1℃时,甲、乙的溶解度均为20g | |
| C. | 温度由t2℃降低到t1℃时,甲溶液析出5g固体 | |
| D. | a,b,c三点中溶质的质量分数由大到小的顺序是:c>a>b |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
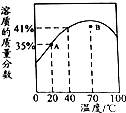
| A. | 40℃时,ZnSO4的溶解度为41g | |
| B. | 点B对应的ZnSO4溶液升温或降温均能达到饱和 | |
| C. | 点A对应的ZnSO4溶液是不饱和溶液 | |
| D. | ZnSO4饱和溶液的溶质质量分数随温度升高而增大 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com