
 事物之间存在联系,找出联系、发现规律是我们学好化学的一种基本方法.
事物之间存在联系,找出联系、发现规律是我们学好化学的一种基本方法.| 规律 | 排序 |
| 示例:标准状况下,密度由大到小 | CO2、C2H4、C2H2、CH4 |
| 元素 | Na | Mg | ① | Si | P | ② | Cl |
| 原子的最外层电子数 | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
| 原子半径(10-10m) | 1.86 | 1.60 | 1.43 | ③ | 1.10 | 1.02 | 0.994 |
| 最高正价 最低负价 | +1 | +2 | ④ | +4 -4 | +5 -3 | ⑤ | +7 -1 |
分析 (1)根据物质的化学式可以判断物质的组成规律;
(2)根据表中提供的信息可以判断相关方面的问题;
(3)根据提供的微观粒子可以判断相关方面的问题;
(4)一氧化碳是目前计入空气污染指数的项目且它的一个分子中含有2个原子,一定条件下能和氧气反应生成二氧化碳;
过氧化氢在二氧化锰催化作用下分解生成水和氧气.
解答 解:(1)CO2、CH4、C2H2(乙炔)、C2H4(乙烯)这四种气体之间存在的另外一个规律并排序如下表所示:
| 规律 | 排序 |
| 碳元素质量分数由高到低 | C2H2、C2H4、CH4、CO2 |
点评 本题主要考查元素周期表方面的知识,只要根据教材中的内容进行分析即可解答.


 新思维寒假作业系列答案
新思维寒假作业系列答案科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 4Fe+3O2$\frac{\underline{\;点燃\;}}{\;}$2Fe2O3 | B. | 2NaOH+CuSO4═Na2SO4+Cu(OH)2↓ | ||
| C. | 2H2O2$\frac{\underline{\;MnO_{2}\;}}{\;}$2H2↑+O2↑ | D. | Fe2O3+2H2SO4═2FeSO4+2H2O |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | Pb2+中质子数比中子数多2 | B. | Pb2+中核电荷数比核外电子数多2 | ||
| C. | Pb2+的最外层电子数是2 | D. | 污水可以过滤后排放到河流中 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

| 物质 | 丁装置中溶液 | 丙装置中溶液 |
| pH | 6.50 | 5.60 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:多选题
| A. | 2Fe+6HCl═2FeCl3+3H2↑ | B. | 4Fe+3O2═2Fe2O3 | ||
| C. | Fe+CuSO4═FeSO4+Cu | D. | 3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
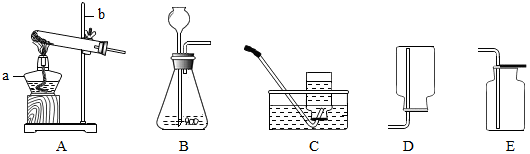
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com