
分析 根据分子的基本特征:分子质量和体积都很小;分子之间有间隔;分子是在不断运动的;同种的分子性质相同,不同种的分子性质不同,可以简记为:“两小运间,同同不不”,结合事实进行分析解答即可.
解答 解:(1)氧气和液氧化学性质相同,是因为它们是由氧分子构成的,同种的分子性质化学相同.
(2)混合物与纯净物,由分子构成的物质,纯净物是由一种分子构成的,混合物是由不同种分子构成的.
(3)墙内开花墙外可以闻到香味,是因为花香中含有的分子是在不断运动的,向四周扩散,使人们闻到花香.
(4)6000L氧气在加压的情况下可装入40L的钢瓶中,是因为分子间有间隔,气体受压后,分子间隔变小.
(5)1滴水中大约有1.67×1021个水分子,说明分子的体积很小.
故答案为:(1)同种的分子性质化学相同;(2)由分子构成的物质,纯净物是由一种分子构成的,混合物是由不同种分子构成的;(3)分子是在不断运动的;(4)分子间有间隔,气体受压后,分子间隔变小;(5)分子的体积很小.
点评 本题难度不大,掌握分子的基本性质(可以简记为:“两小运间,同同不不”)及利用分子的基本性质分析和解决问题的方法是解答此类题的关键.


科目:初中化学 来源: 题型:解答题
 用“侯氏联合制碱法”制得的纯碱(Na2CO3)常含有少量的NaCl.为测定
用“侯氏联合制碱法”制得的纯碱(Na2CO3)常含有少量的NaCl.为测定查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 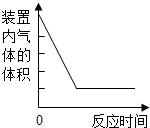 测定空气中氧气的含量 测定空气中氧气的含量 | |
| B. | 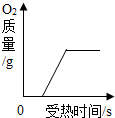 加热高锰酸钾制氧气 加热高锰酸钾制氧气 | |
| C. | 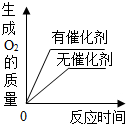 用等质量、等浓度的双氧水分别制取氧气 用等质量、等浓度的双氧水分别制取氧气 | |
| D. | 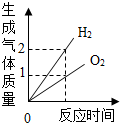 电解水 电解水 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 空气中氧气含量测定的再认识.
空气中氧气含量测定的再认识.| 测量项目 | 实验前 | 实验后 | |
| 烧杯中 水的体积 | 烧杯中 剩余水的体积 | 集气瓶(扣除内容物) 和导管的容积 | |
| 体积/mL | 80.0 | 54.5 | 126.0 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com