
| A. | 按规定停放车辆 | B. | 不随意丢弃废电池 | ||
| C. | 回收使用过的塑料、橡胶 | D. | 在绿化带堆放杂物 |
分析 是不是有利于环境保护,就看这些能源在使用时或使用后随意的丢弃,会不会产生不同程度的污染;
要改善我们生活的环境,可以:植树造林、建人工湖、限制燃煤锅炉的使用、回收废旧电池等.
解答 解:A、按规定停放车辆可以节省空间,并且美观,是利于“创建卫生城市”的行为,不符合题意;
B、不随意丢弃废电池可以保护土壤不受破坏与污染,是利于“创建卫生城市”的行为,不符合题意;
C、回收使用过的塑料、橡胶可以重复利用,并且不会对土壤造成污染,是利于“创建卫生城市”的行为,不符合题意;
D、在绿化带堆放杂物影响市容美观,不是利于“创建卫生城市”的行为,符合题意;
故选D.
点评 此题与生活实际联系紧密,题目涉及的环保知识较多,是当前的考试热点.


 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 保存高铁酸钾时应注意防潮避热 | B. | 高铁酸钾是一种含氧元素的混合物 | ||
| C. | 高铁酸钾中铁元素的化合价为+3价 | D. | 高铁酸钾是一种氧化物 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
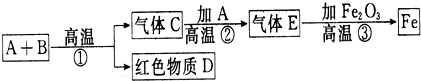
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
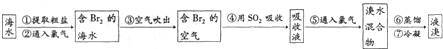
| 温度 溶解度/g 盐 | 10℃ | 20℃ | 30℃ | 40℃ | 50℃ |
| 氯化钠 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 |
| 碳酸氢铵 | 15.8 | 21.0 | 27.0 | ||
| 碳酸氢钠 | 8.1 | 9.6 | 11.1 | 12.7 | |
| 氯化铵 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 某品牌天然矿泉水标签的部分内容如图所示,请用正确的化学用语完成下列问题:
某品牌天然矿泉水标签的部分内容如图所示,请用正确的化学用语完成下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
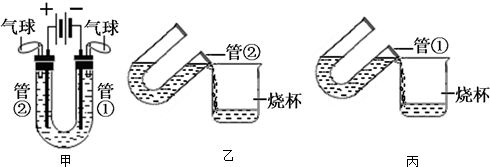
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com