
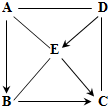
 A、B、C、D、E分别是初中化学常见的五种化合物,其相互反应和转化关系如图所示(“-”表示两端物质间能反应,“→”表示物质间存在转化关系,部分生成物及反应条件已略去).其中D、E均由两种元素组成,且不含相同元素,它们的水溶液均能使石蕊变红;A、C、D、E为不同类别的物质;
A、B、C、D、E分别是初中化学常见的五种化合物,其相互反应和转化关系如图所示(“-”表示两端物质间能反应,“→”表示物质间存在转化关系,部分生成物及反应条件已略去).其中D、E均由两种元素组成,且不含相同元素,它们的水溶液均能使石蕊变红;A、C、D、E为不同类别的物质;分析 根据A、B、C、D、E分别是初中化学常见的五种化合物,D、E均由两种元素组成,且不含相同元素,它们的水溶液均能使石蕊变红,D能转化生成E,所以D可能是盐酸,E可能是二氧化碳,A、C、D、E为不同类别的物质,A和B能与E反应,则A和B为碱,A能转化生成B,则A可能是氢氧化钙,B可能是氢氧化钠,C可能是碳酸钠,然后将推出的物质进行验证即可.
解答 解:(1)A、B、C、D、E分别是初中化学常见的五种化合物,D、E均由两种元素组成,且不含相同元素,它们的水溶液均能使石蕊变红,D能转化生成E,所以D可能是盐酸,E可能是二氧化碳,A、C、D、E为不同类别的物质,A和B能与E反应,则A和B为碱,A能转化生成B,则A可能是氢氧化钙,B可能是氢氧化钠,C可能是碳酸钠,经过验证,推导正确,所以D是HCl,E是CO2;
(2)B与D的反应是盐酸和氢氧化钠反应生成氯化钠和水,化学方程式为:NaOH+HCl═NaCl+H2O;
(3)A→B转化的反应是氢氧化钙和碳酸钠反应生成碳酸钙沉淀和氢氧化钠,化学方程式为:Ca(OH)2+Na2CO3═CaCO3↓+2NaOH,该反应的基本反应类型属于复分解反应.
故答案为:(1)HCl,CO2;
(2)NaOH+HCl═NaCl+H2O;
(3)Ca(OH)2+Na2CO3═CaCO3↓+2NaOH,复分解.
点评 在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质和题中的转化关系推导剩余的物质,最后将推出的各种物质代入转化关系中进行验证即可.


科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
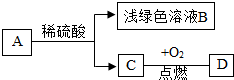 已知,A、B、C、D四种物质之间存在以下转化关系.其中C是单质,D是相对分子质量最小的氧化物.试回答:
已知,A、B、C、D四种物质之间存在以下转化关系.其中C是单质,D是相对分子质量最小的氧化物.试回答:查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | Fe(Cu),足量CuSO4溶液 | B. | CaO(CaCO3),水 | ||
| C. | NaCl〔CaCO3〕,足量水 | D. | CO2(CO),点燃 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
 已知镁原子结构示意图如图所示,请回答:
已知镁原子结构示意图如图所示,请回答:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com