

分析 (1)根据质子数来确定元素,再利用“2-”标在元素符号的右上角来表示离子符号,利用AB2型化合物来分析A、B的化合价,确定元素的位置来分析解答;
(2)根据有毒的含有18个质子的A2B型气体,其水溶液是一种无氧酸可确定是氢硫酸,再利用元素符号及数字来表示3个分子;
(3)根据周期表判断原子的排列规律,然后利用原子序数及最外层电子数来预测元素在周期表中的位置,利用最外层电子数进一步判断离子的结构示意图;
(4)根据周期表判断元素的排列规律.
解答 解:(1)因质子数为8单核原子为氧原子,则利用“2-”标在元素符号的右上角来表示氧离子符号,即带两个单位负电荷且质子数为8的离子为O2-,
由AB2型化合物,则A为+2价,B为-1价,则可以从周期表的第二列和倒数第二列来找合适的元素,如Mg与Cl可形成MgCl2,若A为+4价,B为-2价,则可以从周期表中的倒数第五列和倒数第三列来找合适的元素,如C与O可形成CO2,故答案为:O2-;MgCl2;CO2;
(2)由一种有毒的含有18个质子的A2B型气体,其水溶液是一种无氧酸,则该酸为氢硫酸,其化学式为H2S,化学式可表示1个分子,则在化学式的前面加数字“3”可表示3个分子,故答案为:3H2S;
(3)由周期表可知,在每一横行原子按照质子数由小到大的顺序来排列,即元素从左向右的排列规律是质子数依次增大,质子数为20的元素有4个电子层,最外层电子数为2,则在周期表中的第4个横行和第2个竖列的位置,即在②处,该原子变为离子时失去最外层2个电子而满足最外层8电子的稳定结构,即离子的结构中最外层电子数为8,则元素离子的结构示意图为甲图,故答案为:质子数依次增大,②;
(4)由左到右第二、三周期元素都是质子数依次递增;元素种类由金属元素到非金属元素到稀有气体元素过渡的相同的变化规律.
点评 本题考查学生对元素周期表的认识和应用,将理论与元素、化合物知识结合在一起,难度较大,且考查的知识点较多,学生应熟悉原子的结构及常见物质的性质来解答.


 ABC考王全优卷系列答案
ABC考王全优卷系列答案科目:初中化学 来源: 题型:选择题
| A. | 没有说明用量的,药品可以取任意量 | |
| B. | 使用试管夹时,试管夹要从试管口向下套夹在试管中上部 | |
| C. | 用剩的药品要放回原瓶,不要随意丢弃,以免浪费 | |
| D. | 向试管中滴加液体时,滴管尖嘴不能伸入试管内 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 实验操作 | 实验现象 | 实验结论 |
| 取少量该溶液于试管中,向溶液中滴加足量稀盐酸,并不断振荡. | 有气泡冒出 | 该反应的方程式为 2HCl+Na2CO3═2NaCl+H2O+CO2↑,由此可知该氢氧化钠溶液一定变质了. |
| 实验步骤 | 实验现象 | 实验结论 |
| (1)取少量该溶液于试管中,向溶液中滴加过量的氯化钙溶液,并不断振荡. | 有白色沉淀 | 说明原溶液中一定有碳酸钠. 写出该反应的化学方程式CaCl2+Na2CO3=CaCO3↓+2NaCl. |
| (2)取步骤(1)试管中的少量上层清液,滴加酚酞溶液. | 溶液变红色 | 说明原溶液中一定有氢氧化钠. |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
 已知A、E、F是单质,B、C、D是化合物,它们分别是由碳、氢、氧三种元素中的一种或者几种组成.其中B是相对分子质量最小的氧化物,D物质很不稳定,容易分解生成B和C,它们之间的转化关系如下图所示.
已知A、E、F是单质,B、C、D是化合物,它们分别是由碳、氢、氧三种元素中的一种或者几种组成.其中B是相对分子质量最小的氧化物,D物质很不稳定,容易分解生成B和C,它们之间的转化关系如下图所示.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 电蚊拍一般使用2.4V镍氢电池,工作时电网瞬间产生1850V直流高压电(电流小于10mA,对人畜无害),能将蚊虫吸入电网电毙.如图是一款电蚊拍,请根据图示回答下列问题:
电蚊拍一般使用2.4V镍氢电池,工作时电网瞬间产生1850V直流高压电(电流小于10mA,对人畜无害),能将蚊虫吸入电网电毙.如图是一款电蚊拍,请根据图示回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
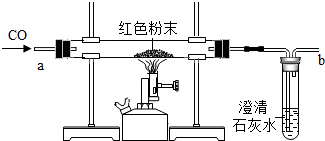 在实验探究课上,老师给了同学们一包红色粉未,该粉末是铜粉和氧化铁粉中的一种或两种.同学们为了确定该粉末的成分,进行如下探究.请你参与他们的探究并回答问题.
在实验探究课上,老师给了同学们一包红色粉未,该粉末是铜粉和氧化铁粉中的一种或两种.同学们为了确定该粉末的成分,进行如下探究.请你参与他们的探究并回答问题.| 实验中可能出现的现象 | 结论 |
| 假设1成立 | |
| 假设2成立 | |
| 假设3成立 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com