
下表是KCl的部分溶解度数据。下列说法正确的是
|
温度(℃) |
0 |
20 |
40 |
60 |
|
溶解度(g) |
27.6 |
34.0 |
40.0 |
45.5 |
A.20℃时,100 g KCl饱和溶液中含34.0 g KCl
B.任何温度下的KCl饱和溶液都不能再溶解其它物质
C.40℃的KCl溶液的浓度一定大于 20℃的KCl饱和溶液的浓度
D.将60℃溶质质量分数为30%的KCl溶液降温至40℃时,有晶体析出
D
【解析】A、20℃时氯化钾的溶解度是34克,指的是在20℃时100g水中溶解氯化钾34g达到饱和,即134gKCl饱和溶液中含KCl34.0g,而不是100g溶液,故A错误;
B、饱和溶液只能指是某种溶质的饱和溶液,而对其他的固体来说,也许是不饱和的,故B错误;
C、40℃的KCl溶液的浓度,题干并没有说明是饱和溶液,故氯化钾的溶液浓度可以很小,有小于20℃的KCl饱和溶液的浓度出现,故C错误;
D、40℃时,氯化钾的溶解度为40g,则溶质质量分数=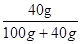 × 100%=28.6%,即在40℃时溶质质量分数只有大于28.6%才会有晶体析出,但30%>28.6%,所以会有晶体析出,故D正确.
× 100%=28.6%,即在40℃时溶质质量分数只有大于28.6%才会有晶体析出,但30%>28.6%,所以会有晶体析出,故D正确.


科目:初中化学 来源: 题型:
| OH- | Cl- | CO32- | SO42- | NO3- | |
| Ca2+ | 微 | 溶 | 难 | 微 | 溶 |
| Ba2+ | 溶 | 溶 | 难 | 难 | 溶 |
| Na+ | 溶 | 溶 | 溶 | 溶 | 溶 |
| H+ | 溶、挥 | 溶、挥 | 溶 | 溶、挥 |
| 问 题 | 实验步骤 | 实验现象 | 结论 | |
| 实验一 | 存在有色离子吗? | 取少量粉末,加水溶解,过滤 | 有白色沉淀生成,滤液无色 | 这种粉末中一定无(填化学式) FeCl3 |
| 实验二 | 实验一中的白色沉淀是什么? | 取少量沉淀,向其中滴加盐酸 | 沉淀部分溶解,有气泡产生 |
白色沉淀是BaSO4和BaCO3 |
| 实验三 | 是否含有KCl | 取少量滤液,滴加硝酸银溶液和稀硝酸 | 产生白色沉淀 | 有KCl存在 |
查看答案和解析>>
科目:初中化学 来源: 题型:
 (1)在初中化学中,我们学习了溶液的有关知识.
(1)在初中化学中,我们学习了溶液的有关知识.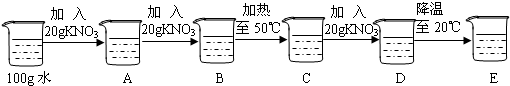
| 物质 | 与众不同的物质 | 理由 |
| KCl K2SO4 K2CO3 BaCO3 |
KCl | KCl中不含氧元素,其他物质中都含有氧元素 |
BaCO3 BaCO3 . |
BaCO3为难溶性盐,其它盐易溶(或“BaCO3为钡盐,其它为钾盐.”) BaCO3为难溶性盐,其它盐易溶(或“BaCO3为钡盐,其它为钾盐.”) . |
查看答案和解析>>
科目:初中化学 来源:湖北省中考真题 题型:填空题
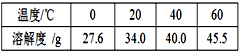
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com