
| A. | 该混合物可能是Zn、A1,w可能是0.2g | |
| B. | 该混合物可能是Zn、Fe,w可能是0.2g | |
| C. | 若混合物为Zn、Cu,w是0.1g,则该混合物中锌的质量分数为50% | |
| D. | 若混合物为Zn、Mg,w是0.1g,则该混合物中锌的质量分数为50% |
分析 假设这6.5 g全部为锌,根据方程式计算出生成氢气为0.2g,根据金属与酸反应时生成氢气的质量=$\frac{金属元素的化合价}{金属的相对原子质量}$×金属的质量,可以推知等质量的Zn、Al、Fe、Mg产生氢气的质量金Al>Mg
>Fe>Zn,进行进一步分析即可.
解答 解:假设6.5g全部为锌,设生成氢气质量为x,则:
Zn+H2SO4═ZnSO4+H2↑
65 2
6.5g x
则$\frac{65}{2}=\frac{6.5g}{x}$,解得:x=0.2g.
同理可计算出6.5g铝、铁与足量硫酸反应产生氢气的质量大于0.2g,
所以可以判断不论是锌中含有铝或是铁,最终生成的氢气的质量都必然大于0.2g,故A、B错误;
C、若锌质量分数为50%,则锌的质量为3.25g,根据上述计算可以知道,3.25g锌能够生成氢气的质量为0.1g,同时铜不能够和稀硫酸反应,所以生成氢气的质量等于0.1g,故C正确;
D、若锌质量分数为50%,则锌的质量为3.25g,根据上述计算可以知道,3.25g锌能够生成氢气的质量为0.1g,同时Mg能够和稀硫酸反应,所以生成氢气的质量大于0.1g,故D错误.
故选:C.
点评 考虑相同质量的金属与酸反应产生氢气的质量的多少与金属的相对原子质量和化合价有关.同价态的金属若相对原子质量越大,产生的氢气质量越小.


科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
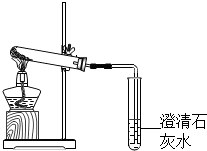 铜火锅是深受人们喜爱的传统产品.但铜制品放置较长时间表面会形成一种绿色有毒的物质.某化学兴趣小组的同学为了探究其成分,从一个久置的废弃铜火锅上取下一些绿色固体进行实验.
铜火锅是深受人们喜爱的传统产品.但铜制品放置较长时间表面会形成一种绿色有毒的物质.某化学兴趣小组的同学为了探究其成分,从一个久置的废弃铜火锅上取下一些绿色固体进行实验.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题

| 营养素 | 每份含量 |
| 蛋白质 | 29.6g |
| 油脂 | 23.5g |
| 糖类 | 104.7g |
| 钠 | 814mg |
| 钙 | 130mg |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 81岁的宁波籍科学家屠呦呦,登上了国际生物大奖“拉斯克奖”的领奖台,因为她发现了青蒿素,一种用于治疗疟疾的药物,挽救了全球特别是发展中国家是数百人的生命,青蒿素的化学式是C15H22O5,如图是该药说明书中的部分内容,则:
81岁的宁波籍科学家屠呦呦,登上了国际生物大奖“拉斯克奖”的领奖台,因为她发现了青蒿素,一种用于治疗疟疾的药物,挽救了全球特别是发展中国家是数百人的生命,青蒿素的化学式是C15H22O5,如图是该药说明书中的部分内容,则:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 1毫升酒精和1毫升水混合后的总体积不等于2毫升 | |
| B. | 1克木炭在1克氧气中充分燃烧生成的二氧化碳质量不等于2克 | |
| C. | 1牛拉力与方向相反的1牛拉力作用在弹簧测力计上读数不等于2牛 | |
| D. | 1欧姆的电阻与1欧姆电阻串联时的总电阻不等于2欧姆 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com