
| 编号 | A | B | C | D |
| 实验设计 | 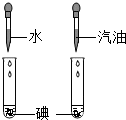 |  |  | 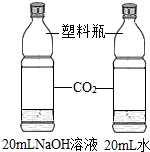 |
| 实验目的 | 探究同种物质在不同溶剂中的溶解性 | 探究分子的运动 | 探究铁生锈的条件 | 探究CO2与NaOH溶液能否发生反应 |
| A. | A | B. | B | C. | C | D. | D |
分析 A、根据碘的溶解性结合控制变量法进行回答;
B、根据分子的运动结合现象进行解答;
C、根据铁生锈的主要条件是铁与水和空气直接接触以及除去铁锈可用盐酸清洗方法进行解答;
D、根据二氧化碳和NaOH溶液反应使瓶内的气压变小进行解答.
解答 解:A、碘溶于汽油,而不溶于水.故实验呈现的不同现象能说明物质的溶解性与溶剂种类有关,故方法正确;
B、浓氨水和酚酞试液的烧杯放入倒扣的大烧杯中时,会看到酚酞试液变红的现象,能够说明氨气的分子从氨水的烧杯进入到盛有酚酞试液的烧杯,能够探究分子运动,故选项实验能达到实验目的,方法正确;
C、对于实验C,一段时间试管①②试管内铁钉都不生锈,说明试管内只提供水或氧气都不能生锈,同时没有证明二者同时存在能否生锈,因此不能得出:铁生锈需要和氧气接触;故方法错误;
D、二氧化碳和与水、氢氧化钠都反应,通过实验对比塑料瓶变瘪的程度说明二氧化碳能够和氢氧化钠反应;故方法正确;
故选:C.
点评 此题是一道实验设计题,解题的关键是掌握分子的性质、铁生锈的条件、二氧化碳的性质、物质的溶解性,并进行知识的大胆迁移,只有这样才能顺利解题.


科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
 以物质的类别为横坐标,化合价为纵坐标绘制的图象,如图是铁的价类图,Y物质为( )
以物质的类别为横坐标,化合价为纵坐标绘制的图象,如图是铁的价类图,Y物质为( )| A. | FeO | B. | Fe(OH)2 | C. | Fe3O4 | D. | FeSO4 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
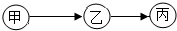 甲、乙、丙为初中常见物质,其转化关系如图(“→”表示由一种物质转化成另一种物质,反应条件、部分反应物和生成物已略去).
甲、乙、丙为初中常见物质,其转化关系如图(“→”表示由一种物质转化成另一种物质,反应条件、部分反应物和生成物已略去).查看答案和解析>>
科目:初中化学 来源: 题型:推断题
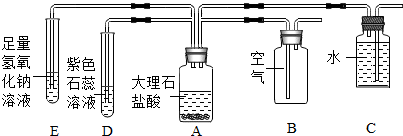
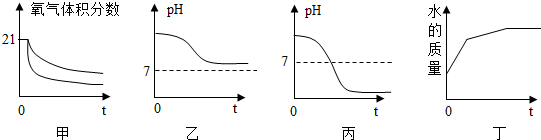
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
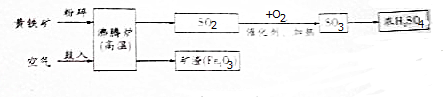
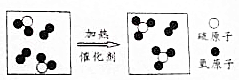
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 碘酒是混合物-由不同种分子构成 | |
| B. | 气体受热膨胀-温度升高,分子自身体积变大 | |
| C. | 过氧化氢溶液加入二氧化锰能生成氧气,水中加入二氧化锰不能生成氧气-不同分子,性质不同 | |
| D. | 瓜果飘香-分子在不停地运动 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com