
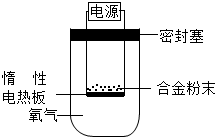
 镁是一种活泼金属,除了能与氧气反应,还可以与氮气、二氧化碳等反应.为测定镁铝合金(不含其他元素)中镁的质量分数,称量ag镁铝合金粉末,放在如图所示装置的惰性电热板上,通电使其充分灼烧.下列关于该实验的说法正确的是( )
镁是一种活泼金属,除了能与氧气反应,还可以与氮气、二氧化碳等反应.为测定镁铝合金(不含其他元素)中镁的质量分数,称量ag镁铝合金粉末,放在如图所示装置的惰性电热板上,通电使其充分灼烧.下列关于该实验的说法正确的是( )| A. | ④⑤ | B. | ①②⑤ | C. | ③④⑤ | D. | ①②③⑤ |
分析 根据镁是一种活泼金属,除了能与氧气反应,还可以与氮气,二氧化碳等反应,所以不能用空气代替氧气;欲计算镁的质量分数,该实验中还需测定的一种数据是:完全反应后生成的固体的质量;镁铝合金在电热板上,通电使其充分灼烧生成氧化镁、氧化铝进行分析.
解答 解:①为了使其充分灼烧,氧气要保证充足,故正确;
②实验结束后一定要再次称量剩余固体质量,再通过其它操作可以计算镁铝合金中镁的质量分数,故正确;
③用空气代替氧气对实验有影响,这是因为高温条件下,镁还能够和氮气、二氧化碳等反应,故错误;
④灼烧后的固体为氧化镁和氧化铝的混合物,故错误;
⑤假设ag镁铝合金粉末,全部是镁,可以生成氧化镁为x
2Mg+O2$\frac{\underline{\;点燃\;}}{\;}$2MgO
48 80
ag x
$\frac{48}{ag}$=$\frac{80}{x}$
x=$\frac{5a}{3}$
假设ag镁铝合金粉末,全部是铝,可以生成氧化铝为y
4Al+3O2$\frac{\underline{\;点燃\;}}{\;}$2Al2O3,
54 204
ag y
$\frac{54}{ag}$=$\frac{204}{y}$
y=$\frac{17a}{9}$
所以充分灼烧后固体的质量介于$\frac{5}{3}$a~$\frac{17}{9}$a之间,故正确.
故选:B.
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.


 孟建平小学滚动测试系列答案
孟建平小学滚动测试系列答案 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
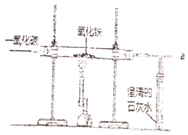
 如图所示是一罐刚开启的饮料,其饮料成分如图所示,某位同学根据物质的组成,将这四种物质分为甲、乙两类(如表所示).下列对分类结果判断正确的是( )
如图所示是一罐刚开启的饮料,其饮料成分如图所示,某位同学根据物质的组成,将这四种物质分为甲、乙两类(如表所示).下列对分类结果判断正确的是( )| 类别 | 物质 |
| 甲 | 水、二氧化碳 |
| 乙 | 蔗糖、葡萄糖 |
| A. | 甲为氧化物,乙为有机物 | B. | 甲为酸、乙为盐 | ||
| C. | 甲为单质,乙为化合物 | D. | 甲为化合物,乙为氧化物 |
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
| 试验次序 | 第1次 | 第2次 | 第3次 | 第4次 |
| 所取样品的质量/g | 50.0 | 50.0 | 50.0 | 50.0 |
| 加入稀硫酸的质量/g | 20.0 | 40.0 | 60.0 | 80.0 |
| 生成气体的质量/g | 0.2 | 0.4 | 0.5 | 0.5 |
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 芬太奴的每一个分子中含有47个原子 | |
| B. | 芬太奴是由碳、氢、氧、氮四种元素组成的物质 | |
| C. | 芬太奴中碳的质量分数最大 | |
| D. | 芬太奴中碳、氢、氧、氮的原子个数比为240:24:28:16 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com