
分析 首先根据题意确定物质的化学名称,然后根据书写化学式的方法和步骤写出物质的化学式即可.
解答 解:(1)澄清石灰水的溶质是氢氧化钙,其化学式为:Ca(OH)2.
(2)可用于焙制糕点时的发酵粉的是碳酸氢钠,其化学式为:NaHCO3.
(3)可用于治疗胃酸过多的是氢氧化铝(或碳酸氢钠),其化学式为:Al(OH)3(或NaHCO3).
(4)氧化钙能与水反应,是能作干燥剂的物质,其化学式为:CaO.
(5)硝酸钾中含有钾元素和氮元素,属于复合肥,其化学式为:KNO3.
故答案为:(1)Ca(OH)2;(2)NaHCO3;(3)Al(OH)3(或NaHCO3);(4)CaO;(5)KNO3.
点评 本题难度不大,熟练掌握常见物质的性质、用途、组成及化学式的书写是正确解答此类题的关键所在.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:解答题
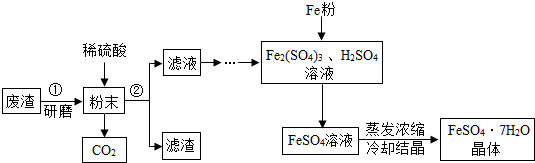
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
| 时间/h | 2 | 4 | 6 | 8 | 10 | 12 | 24 |
| 实验1 | 不褪色 | 不褪色 | 不褪色 | 由稍褪色到褪色且速度逐渐加快 | |||
| 实验2 | 不褪色 | 不褪色 | 不褪色 | 不褪色 | 不褪色 | 褪色且速度加快 | |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 都需要加热 | B. | 都需要催化剂 | ||
| C. | 都有元素化合价的升降 | D. | 都有氧化物生成 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
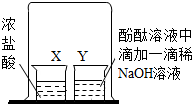 向小烧杯Y中加入一定量的酚酞溶液,并滴加一滴稀NaOH溶液,然后做如图所示实验.请回答:
向小烧杯Y中加入一定量的酚酞溶液,并滴加一滴稀NaOH溶液,然后做如图所示实验.请回答:查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 酸中一定含氧元素 | B. | 含氧的化合物一定是氧化物 | ||
| C. | 盐中一定含金属元素 | D. | 碱中一定含氢元素和氧元素 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com