
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解

| 猜想 | 实验操作 | 可能的现象 | 结论 |
| 小华猜想 | 取适量黑色粉末A 用磁铁吸引 | 粉末全部被吸引 | 猜想正确 |
| 你的猜想 | 取适量黑色粉末B用磁铁吸引 取适量黑色粉末B用磁铁吸引 |
粉末不能被吸引 粉末不能被吸引 |
你的猜想 正确 |
查看答案和解析>>
科目:初中化学 来源: 题型:
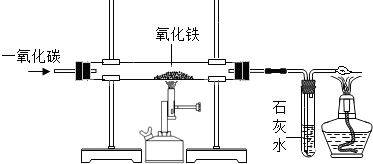 铁及其化合物在日常生活中随处可见.
铁及其化合物在日常生活中随处可见.
| ||
| ||
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
| ||
. |
| ||
. |
| ||
. |
| ||
. |
查看答案和解析>>
科目:初中化学 来源: 题型:
 铝、铁、铜是人类广泛使用的三种金属,与我们生活息息相关.
铝、铁、铜是人类广泛使用的三种金属,与我们生活息息相关.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com