
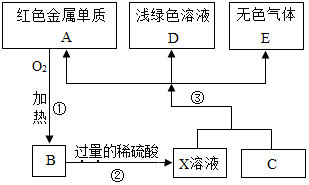
 A、B、C、D、E为初中化学常见的物质,其中A、C为金属单质,E为非金属单质,图是它们之间的相互转化关系.请回答:
A、B、C、D、E为初中化学常见的物质,其中A、C为金属单质,E为非金属单质,图是它们之间的相互转化关系.请回答:分析 根据A是红色金属单质说明A是铜,铜与氧气反应生成氧化铜,所以B是氧化铜,氧化铜与硫酸反应生成硫酸铜和水,再根据亚铁离子溶液是浅绿色再进一步进行分析,根据加入过量的稀硫酸来考虑产生气体的原因.
解答 解:(1)铜是红色固体且属于金属单质,所以由A是红色金属单质说明A是铜,铜与氧气反应生成氧化铜,所以B是氧化铜,氧化铜与硫酸反应生成硫酸铜和水,所以X溶液中含有过量的硫酸和硫酸铜,因为亚铁离子溶液是浅绿色,所以D中含有亚铁离子,因为C和X中的物质反应生成铜和亚铁盐,且C属于金属单质,所以C是铁,铁与硫酸铜反应生成铜和硫酸亚铁;铁与过量的硫酸反应生成硫酸亚铁和氢气,所以D是硫酸亚铁;
(2)在第②步中加入的稀硫酸是过量的,所以铁与过量的硫酸反应,生成硫酸亚铁和氢气.
故答案为:(1)Fe;FeSO4;(2)(2)H2+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+H2O;(3)铁与过量的稀硫酸反应,生成硫酸亚铁和氢气.
点评 本题考查了常见物质的推断,解题时往往需要从题目中挖出一些明显或隐含的条件,抓住突破口(突破口往往是现象特征、反应特征及结构特征),导出结论,最后别忘了把结论代入原题中验证,若“路”走得通则已经成功.


 状元及第系列答案
状元及第系列答案 同步奥数系列答案
同步奥数系列答案科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 水和冰混合、澄清石灰水 | B. | 净化后的空气、氧化镁 | ||
| C. | 生锈的铁钉、液氧 | D. | 氧化铜、氧化镁 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
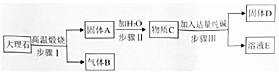 小型化工厂常以纯碱和大理石为主要原料,按以下工艺流程生产烧碱(NaOH).
小型化工厂常以纯碱和大理石为主要原料,按以下工艺流程生产烧碱(NaOH).查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | ①③ | B. | ②④ | C. | ①② | D. | ③④ |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 硝酸银溶液、铁片、铜片 | B. | 硝酸铜溶液、硝酸银溶液、铁片 | ||
| C. | 铜片、硝酸亚铁溶液、硝酸银溶液 | D. | 铁片、稀盐酸、银片、铜片 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com