
分析 (1)含有氮元素的化肥属于氮肥;铵态氮肥不能和显碱性物质混合使用;含有碳元素的化合物属于有机物;根据物质的化学式可以计算某种元素的质量分数.
(2)根据元素化合价的表示方法:确定出化合物中所要标出的元素的化合价,然后在其化学式该元素的上方用正负号和数字表示,正负号在前.
(3)根据铵盐遇碱性物质易放出氨气分析回答;
(4)根据水体污染的原因分析.
解答 解:(1)尿素和尿素都是含有氮元素的化肥,均属于氮肥.
故答案是:B.
(2)硝酸铵中铵根显+1价,氢元素显+1价,设氮元素的化合价为x,则x+(+1)×4=+1,故x=-3,硝酸根显-1价,其中的氧元素显-2价,设氮元素的化合价为y,则y+(-2)×3=-1,则y=+5,所以硝酸铵中氮元素的化合价是-3;+5.
故答案是:+3;-5.
(3)硝酸铵不能与碱性物质混合使用的原因是:硝酸铵能与碱性物质反应产生氨气,降低肥效;答案:硝酸铵能与碱性物质反应产生氨气,降低肥效.
(4)过量使用化肥会造成水体污染.
故答案是:可能会造成水体污染(合理即可).
点评 本题难度不大,掌握化肥和物质的分类方法及其元素化合价的计算方法是解题的关键.


科目:初中化学 来源: 题型:选择题
| A. | 前者质量变小,后者质量变大,二者溶质的质量分数都变小 | |
| B. | 前者质量变大,后者质量变小,二者溶质的质量分数都变大 | |
| C. | 前者质量变大,后者质量变小,二者溶质的质量分数都变小 | |
| D. | 前者质量变小,后者质量变大,二者溶质的质量分数都变大 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
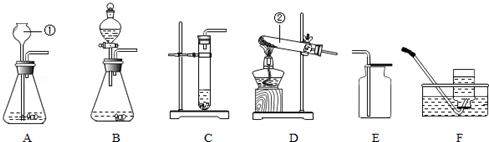
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | HCl、BaCl2、Na2CO3、过滤、NaOH | B. | Na2CO3、NaOH、BaCl2、过滤、HCl | ||
| C. | BaCl2、NaOH、Na2CO3、过滤、HCl | D. | Na2CO3、BaCl2、NaOH、过滤、HCl |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
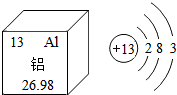 铝元素与人类关系密切.
铝元素与人类关系密切.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com