
| A. | 滤纸上有 Ag、Cu,滤液中只有Zn2+、Mg2+ | |
| B. | 滤纸上有 Ag,滤液中有Ag+、Cu2+、Zn2+、Mg2+ | |
| C. | 滤纸上有 Ag、Cu,滤液中有Ag+、Zn2+、Mg2+ | |
| D. | 滤纸上有 Ag、Cu、Zn,滤液中有Zn2+、Mg2+ |
分析 根据在金属活动性顺序中,镁>锌>铜>银,位置在前的金属能将位于其后的金属从其盐溶液中置换出来进行分析.
解答 解:AgNO3、Cu(NO3)2、Mg(NO3)2 的混合溶液中加入一些锌粉,镁>锌>铜>银,锌不会与硝酸镁反应,所以滤液中一定含有Mg2+,锌与硝酸银反应生成硝酸锌和银,锌与硝酸铜反应生成硝酸锌和铜,生成的铜与硝酸银能反应生成硝酸铜和银.
A、当锌粉量不足时,只与部分硝酸银反应,生成银,仍有硝酸银剩余,因此滤渣只有银,滤液含有硝酸银、硝酸铜、硝酸锌及硝酸镁,故说法正确;
B、当锌粉适量时,能与混合液中的硝酸银和硝酸铜恰好完全反应,生成银和铜,因此滤渣只有银和铜,滤液含有硝酸锌和硝酸镁,故说法正确;
C、锌会先与硝酸银反应生成硝酸锌和银,再与硝酸铜反应生成硝酸锌和铜,因此滤渣含有铜,则滤液一定不能含有硝酸银,故说法错误;
D、当锌粉过量时,与混合液中的硝酸银和硝酸铜完全反应,生成银和铜,锌有剩余,因此滤渣中含有银、铜、锌,滤液中含有硝酸锌和硝酸镁,故说法正确;
故选:C.
点评 本题考查了金属活动性顺序的应用,完成此题,可以依据金属活动性顺序的意义进行分析,要求学生会利用金属活动性顺序表的应用,来判断反应能否发生及反应的程度.


 教育世家状元卷系列答案
教育世家状元卷系列答案 黄冈课堂作业本系列答案
黄冈课堂作业本系列答案 单元加期末复习先锋大考卷系列答案
单元加期末复习先锋大考卷系列答案科目:初中化学 来源: 题型:选择题
| A. | 二氧化碳是有二氧化碳分子构成的 | |
| B. | 一个二氧化碳分子是由一个碳原子和两个氧原子构成的 | |
| C. | 二氧化碳是有碳、氧两种元素组成的 | |
| D. | 一个二氧化碳分子是由碳元素和氧元素组成的 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 镁条易折断 | B. | 武德合金的熔点约为69℃ | ||
| C. | 铜具有良好的导电性 | D. | 铜绿能与稀盐酸反应产生气泡 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 物质 | 甲 | 乙 | 丙 | 丁 |
| 反应前质量(g) | 4 | 1 | 42 | 10 |
| 反应后质量(g) | 待测 | 20 | 6 | 31 |
| A. | 反应后,甲的“待测”值应为0 | B. | 丁是生成物 | ||
| C. | 该反应是复分解反应 | D. | 反应中甲与乙的质量比是4:19 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验步骤 | 实验现象 | 实验结论 |
| 猜想正确 |
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量滤液于试管中,滴加少量稀盐酸 | 无明显现象 | 猜想正确 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | ①③ | B. | ②⑤ | C. | ③④ | D. | ④⑤ |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
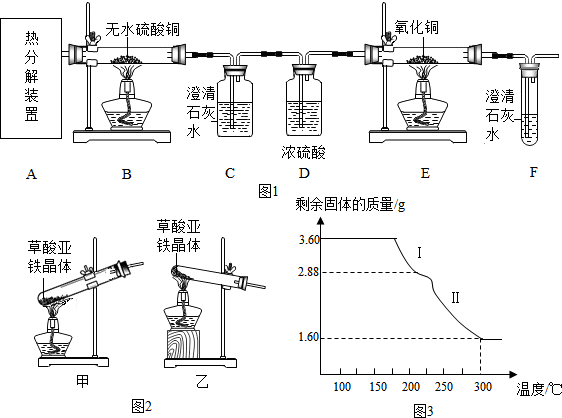
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com