
| A. | C24H38O4中碳、氢、氧元素质量比为12:19:2 | |
| B. | 邻苯二甲酸二辛酯中碳元素的质量分数最大 | |
| C. | C24H38O4由24个碳原子、38个氢原子、4个氧原子构成 | |
| D. | 邻苯二甲酸二辛酯属于氧化物 |
分析 A、根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析解答.
B、根据化合物中元素的质量分数公式,进行分析判断.
C、根据邻苯二甲酸二辛酯的微观构成进行分析判断.
D、氧化物是只含有两种元素且其中一种元素是氧元素的化合物,据此进行分析判断
解答 解:A、C24H38O4中碳、氢、氧元素质量比为(12×24):38:(16×4)=144:19:32,故选项说法错误.
B、邻苯二甲酸二辛酯中碳原子的相对原子质量之和为12×24,氢原子的相对原子质量之和为1×38,氧原子的相对原子质量之和为16×4,碳元素的相对原子质量之和最大,则碳元素的质量分数最高,故选项说法正确.
C、1个C24H38O4分子是由24个碳原子、38个氢原子、4个氧原子构成的,故选项说法错误.
D、邻苯二甲酸二辛酯中含有碳、氢、氧三种元素,不属于氧化物,故选项说法错误.
故选:B
点评 本题难度不大,考查同学们结合新信息、灵活运用化学式的含义与有关计算进行分析问题、解决问题的能力.


科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
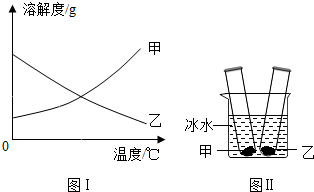 甲、乙两种固体物质的溶解度曲线如图Ⅰ所示.常温下,分别向装有适量甲、乙物质的两支试管里加入等量的蒸馏水,充分振荡后,两支试管底部均有未溶解的固体;再将两支试管放入盛有冰水混合物的烧杯里,如图Ⅱ所示.关于该实验,下列说法中正确的是( )
甲、乙两种固体物质的溶解度曲线如图Ⅰ所示.常温下,分别向装有适量甲、乙物质的两支试管里加入等量的蒸馏水,充分振荡后,两支试管底部均有未溶解的固体;再将两支试管放入盛有冰水混合物的烧杯里,如图Ⅱ所示.关于该实验,下列说法中正确的是( )| A. | 甲、乙两物质的溶解度都增大 | |
| B. | 两支试管里剩余的固体都增多 | |
| C. | 乙溶液中溶质的质量分数增大 | |
| D. | 装有甲物质的试管中剩余的固体减少 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
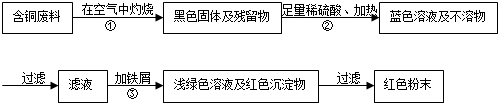
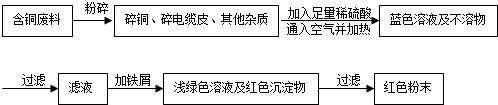
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | m×a% g | B. | (m-w) g | C. | (m-w)×a% g | D. | ( m+w)×a% g |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com