
 如图为甲、乙两物质(均不含结晶水)的溶解度曲线,下列说法正确的是( )
如图为甲、乙两物质(均不含结晶水)的溶解度曲线,下列说法正确的是( )| A. | 20℃时,100g甲溶液中含甲物质的质量为25g | |
| B. | 将甲物质的溶液从50℃降温到30℃时一定都有晶体析出 | |
| C. | 20℃时,等质量甲、乙饱和溶液中含溶质的质量相等 | |
| D. | 将甲、乙两种物质的溶液分别从50℃降温到20℃时,溶液中溶质质量分数均为25% |
分析 根据固体的溶解度曲线可以:①查出某物质在一定温度下的溶解度,从而确定物质的溶解性,②比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质的质量分数的大小,③判断物质的溶解度随温度变化的变化情况,从而判断通过降温结晶还是蒸发结晶的方法达到提纯物质的目的.
解答 解:A、20℃时,甲物质的溶解度是25g,所以125g甲溶液中含甲物质的质量为25g,故A错误;
B、甲物质的溶解度随温度的升高而增大,所以将甲物质的溶液状态不能确定,从50℃降温到30℃时不一定有晶体析出,故B错误;
C、20℃时,甲、乙物质的溶解度相等,所以等质量甲、乙饱和溶液中含溶质的质量相等,故C正确;
D、20℃时,甲、乙物质的溶解度是25g,所以将甲、乙两种物质的溶液分别从50℃降温到20℃时,饱和溶液中溶质质量分数均为:$\frac{25g}{125g}$×100%=20%,若不饱和,溶质质量分数小于20%,故D错误.
故选:C.
点评 本题难度不是很大,主要考查了固体的溶解度曲线所表示的意义,及根据固体的溶解度曲线来解决相关的问题,从而培养分析问题、解决问题的能力.


科目:初中化学 来源: 题型:选择题
| A. | 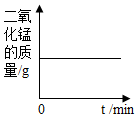 加热KClO3和MnO2固体混合物 | |
| B. | 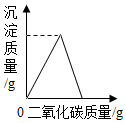 向Ca(OH)2溶液中通入CO2至过量 | |
| C. | 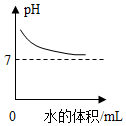 向一定浓度的NaOH溶液中加水稀释 | |
| D. | 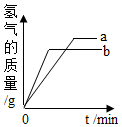 将等质量的Mg和Al分别与过量等浓度的盐酸反应,则a为Mg,b为Al |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 将锌片放入硝酸银溶液 | B. | 将铜片放入稀硫酸 | ||
| C. | 将铜片放入硝酸银溶液 | D. | 将锌片放入稀硫酸 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 天然气是混合物 | |
| B. | 甲烷是由一个碳原子和四个氢原子构成的 | |
| C. | 甲烷是由两种非金属组成的 | |
| D. | 甲烷中碳氢元素的质量比为1:4 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 淮南采集煤矿矿井内保持通风良好,严禁烟火 | |
| B. | 铜陵有色金属公司有计划、合理开采矿物,保护金属资源 | |
| C. | 淮北利用当地丰富的煤炭资源,大力发展火力发电 | |
| D. | 江淮汽车发展新能源汽车,并逐步完善废旧电池回收市场 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
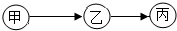 甲、乙、丙为初中化学常见物质,其转化关系如图所示(“→”表示由一种物质转化成另一种物质,其中部分反应物、生成物及反应条件已略去).
甲、乙、丙为初中化学常见物质,其转化关系如图所示(“→”表示由一种物质转化成另一种物质,其中部分反应物、生成物及反应条件已略去).查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com