
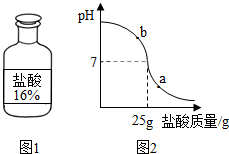
| 100g-20g |
| 1g/mL |
| 36.5 |
| x |
| 40 |
| 4g |
| 3.65g |
| 25g |


科目:初中化学 来源: 题型:
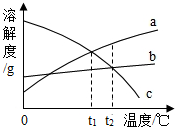 a、b、c三种不含结晶水的固体物质的溶解度曲线如图.取等质量 t2℃的 a、b、c 三种物质的饱和溶液,分别蒸发等量水后恢复至 t2℃.下列说法不正确的是( )
a、b、c三种不含结晶水的固体物质的溶解度曲线如图.取等质量 t2℃的 a、b、c 三种物质的饱和溶液,分别蒸发等量水后恢复至 t2℃.下列说法不正确的是( )| A、原饱和溶液中,溶质的质量分数a>b=c |
| B、恢复至t2℃时,析出溶质的质量a=b=c |
| C、恢复至t2℃时,三种溶液一定都是饱和溶液 |
| D、若继续降温至 t1℃,c溶液可能变成不饱和溶液 |
查看答案和解析>>
科目:初中化学 来源: 题型:
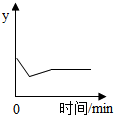 向一定量的饱和石灰水中加入少量生石灰,y随时间的变化趋势如图所示,则y可表示( )
向一定量的饱和石灰水中加入少量生石灰,y随时间的变化趋势如图所示,则y可表示( )| A、??①②③ | B、?①④ |
| C、??②③ | D、①③④ |
查看答案和解析>>
科目:初中化学 来源: 题型:
| A、将NaOH固体放入小烧杯中,用托盘天平称取2.0g NaOH固体 |
| B、用500mL量筒量取98.0mL水 |
| C、将称取的NaOH固体直接倒入量筒中溶解 |
| D、10mL2%的NaOH溶液中加入10mL水稀释得到1% NaOH溶液 |
查看答案和解析>>
科目:初中化学 来源: 题型:
| 物质 | NaCl | NaOH | Na2CO3 | NaHCO3 |
| 20°C溶解度/g | 36 | 109 | 21.5 | 9.6 |
| 水溶液的pH | 7 | 14 | 11 | 9 |
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
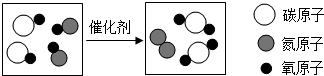 用化学符号和数字填空:
用化学符号和数字填空:查看答案和解析>>
科目:初中化学 来源: 题型:
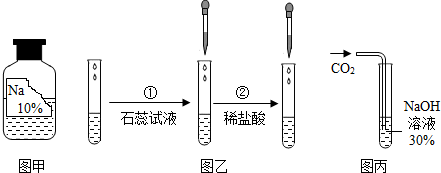
| A、氢化钙的化学性质稳定 |
| B、①中发生化合反应,②中发生复分解反应 |
| C、氢化钙作为能源提供剂是因为与水反应能生成氢气 |
| D、氢化钙可用于干燥潮湿的二氧化碳、氯化氢等气体 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com