
分析 (1)根据反应原理找出反应物、生成物、反应条件,根据化学方程式的书写方法、步骤进行书写即可;
(2)①根据反应物、生成物和条件书写方程式;
②从碳酸盐检验方法去分析解答;
③A.上述设想中的原料是二氧化碳、氧化钙,原料易得,反应过程中二氧化碳和氧化钙既是步骤1的反应物,又是步骤2的生成物,可以循环使用去分析解答;
B.反应的反应条件是光照和加热,太阳能也能提供热量去分析解答;
C.从遮光的地方及阴天没有太阳时就不能反应去分析解答;
(3)根据微粒之间有间隔解答;
(4)根据反应物和只生产一种物质的特点以及质量守恒定律可判断生成物;根据反应物和生成物可以书写化学方程式;
解答 解:
(1)上述反应中两个反应的反应物相同,但得到的产物却完全不同,原因是反应条件不同;绿色植物光合作用反应的化学方程式为:6CO2+6H2O $\frac{\underline{\;叶绿素\;}}{光照}$C6H12O6+6O2;能量转化为光能转化为化学能;
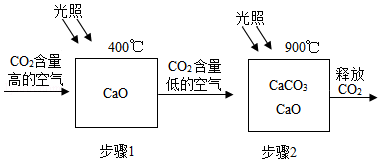
(2)①用化学方程式表示使空气中CO2含量减少的原因是CaO+CO2$\frac{\underline{\;400℃\;}}{光照}$CaCO3;
②碳酸钙属于碳酸盐,碳酸盐的检验可加入稀盐酸,如果有二氧化碳气体产生,说明含有碳酸盐;
③A.上述设想中的原料是二氧化碳、氧化钙,原料易得,反应过程中二氧化碳和氧化钙既是步骤1的反应物,又是步骤2的生成物,可以循环使用故正确;
B.反应的反应条件是光照和加热,太阳能也能提供热量;故正确;
C.遮光的地方及阴天没有太阳时就不能反应;故错误;
(3)二氧化碳能够压缩成液态的原因是二氧化碳分子之间有间隔;
(4)因为是二氧化碳和氢气反应,所以生成物中碳原子和氧原子的个数比应该是1:2.甲酸CH2O2中碳原子和氧原子的个数比是1:2;根据反应物、生成物写出化学反应式,配平即可,方程式为:CO2+H2═CH2O2.属于化合反应.
答案:
(1)反应条件不同;6CO2+6H2O $\frac{\underline{\;叶绿素\;}}{光照}$C6H12O6+6O2;
(2)①CaO+CO2$\frac{\underline{\;400℃\;}}{光照}$CaCO3;②取少量固体于试管中,滴加过量的稀盐酸,观察到有气泡产生,则分解不完全;③C;
(3)二氧化碳分子之间有间隔;
(4)化合反应.;C.
点评 本题考查了二氧化碳的有关性质及方程式的书写,完成此题,可以依据已有的知识进行.


 习题精选系列答案
习题精选系列答案科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
 人类的生活和生产都离不开金属.
人类的生活和生产都离不开金属.查看答案和解析>>
科目:初中化学 来源: 题型:填空题
 如图所示是液态二氧化碳灭火器,请回答下列问题.
如图所示是液态二氧化碳灭火器,请回答下列问题.查看答案和解析>>
科目:初中化学 来源: 题型:推断题
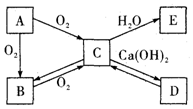 已知A、B、C、D、E是初中化学中五种常见的纯净物,五种物质中只有A为黑色固体物质,B、C所含元素相同,相对分子质量:C>B;由于条件不同,A和O2反应可生成B也可生成C.五种物质在一定条件下的转化关系如图所示(“→”表示物质间可转化,部分反应物和生成物没有列出).试推断并回答相关问题:
已知A、B、C、D、E是初中化学中五种常见的纯净物,五种物质中只有A为黑色固体物质,B、C所含元素相同,相对分子质量:C>B;由于条件不同,A和O2反应可生成B也可生成C.五种物质在一定条件下的转化关系如图所示(“→”表示物质间可转化,部分反应物和生成物没有列出).试推断并回答相关问题:查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
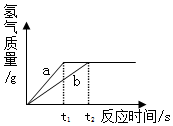
 小峰和小刚阅读试剂标签后发现,市场销售的高锰酸钾晶体纯度高达99.5%,含水量可以忽略不计,为探究“试管放置方式对高锰酸钾制取氧气速度和体积的影响”,他俩设计了制取氧气的直立型装置(如图),并与斜卧型装置比较,在气密性良好的装置中分别加入5.0克高锰酸钾晶体,用同一酒精灯 分别加热,用同一型号的集气瓶收集气体,每组实验进行五次,实验数据取平均值后记录如下表:
小峰和小刚阅读试剂标签后发现,市场销售的高锰酸钾晶体纯度高达99.5%,含水量可以忽略不计,为探究“试管放置方式对高锰酸钾制取氧气速度和体积的影响”,他俩设计了制取氧气的直立型装置(如图),并与斜卧型装置比较,在气密性良好的装置中分别加入5.0克高锰酸钾晶体,用同一酒精灯 分别加热,用同一型号的集气瓶收集气体,每组实验进行五次,实验数据取平均值后记录如下表:| 装置类型 | 直立型 | 斜卧型 |
| 收集1瓶氧气所需时间/秒 | 59 | 68 |
| 收集2瓶氧气所需时间/秒 | 95 | 108 |
| 收集氧气的总体积/毫升 | 525 | 476 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 保鲜水产品可用甲醛溶液来浸泡 | |
| B. | 塑料、橡胶均属于有机合成材料 | |
| C. | 霉变的谷物清洗后可放心食用 | |
| D. | 焙制糕点时常添加含小苏打的发酵粉 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 阳离子 | Ba2+ | Na+ | Fe3+ | Mg2+ |
| 阴离子 | Cl- | NO3- | SO4- | OH- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com