
| 选项 | 实验目的 | 方案 |
| A | 检验氢氧化钠是否部分变质 | 加入氯化钙溶液 |
| B | 制备氢氧化钾 | 向氢氧化镁中加入碳酸钾 |
| C | 检验氯离子 | 先加入稀硝酸,再滴加硝酸银溶液 |
| D | 除去氧化钙中的碳酸钙 | 加入稀盐酸至不再产生气泡,过滤 |
| A. | A | B. | B | C. | C | D. | D |
分析 A、根据碳酸钠和氯化钙反应会生成碳酸钙沉淀和氯化钠进行分析;
B、根据氢氧化镁是不溶性碱,不会与碳酸钾反应进行分析;
C、根据加入硝酸可以排除碳酸根离子的干扰,加入硝酸银会生成白色沉淀,说明含有氯离子进行分析;
D、根据盐酸会与氧化钙、碳酸钙反应进行分析.
解答 解:A、取样品,加入氯化钙溶液,有白色沉淀后生成,说明氢氧化钠变质,但是不能检验氢氧化钠是部分变质,还是全部变质,故A错误;
B、氢氧化镁是不溶性碱,不会与碳酸钾反应,故B错误;
C、加入硝酸可以排除碳酸根离子的干扰,加入硝酸银会生成白色沉淀,说明含有氯离子,故C正确;
D、盐酸会与氧化钙、碳酸钙反应,除去了杂质和主要物质,故D错误.
故选:C.
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:推断题
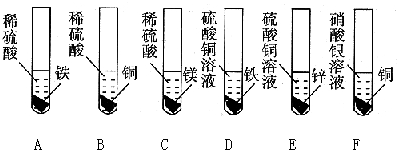
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
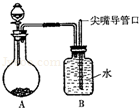 小茜设计了一个趣味实验装置(见图),其气密性良好.若要使B中尖嘴导管有“喷泉”产生,则A中加入的固体和液体不可行的是( )
小茜设计了一个趣味实验装置(见图),其气密性良好.若要使B中尖嘴导管有“喷泉”产生,则A中加入的固体和液体不可行的是( )| A. | 氧化钙和水 | B. | 硝酸铵和水 | ||
| C. | 二氧化锰和过氧化氢溶液 | D. | 锌粒和硫酸溶液 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
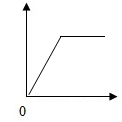 如表各选项与如图所示曲线相符的是( )
如表各选项与如图所示曲线相符的是( )| 序号 | 横坐标 | 纵坐标 |
| A | 向一定量稀硫酸中加入锌粉的质量 | 溶液中氢元素的质量 |
| B | 向一定量的氢氧化钠和碳酸钠混合溶液中加入稀盐酸的质量 | 产生气体的质量 |
| C | 向混有盐酸的硫酸钠溶液中加入氢氧化钡溶液的质量 | 生成沉淀的质量 |
| D | 在一定温度下,向一定量不饱和硝酸钾溶液中加入硝酸钾固体的质量 | 溶液中溶质的质量分数 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com