
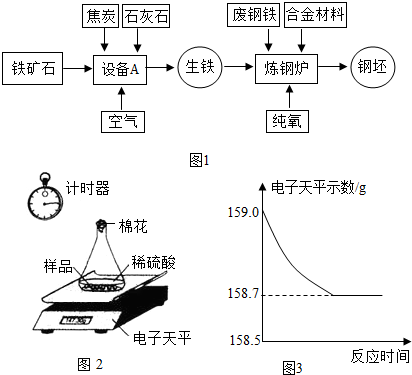
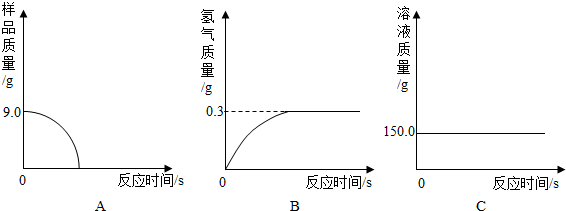
分析 根据反应记录数据,完全反应放出氢气质量=159.0g-158.7g=0.3g,加入稀硫酸的质量=159.0g-44.1g-9.0g=105.9g;结合反应的化学方程式,由生成氢气的质量计算生铁中铁的质量、反应生成硫酸亚铁的质量等,完成分析和计算.
解答 解:①由于生铁样品中的杂质不溶于水且不与酸发生反应,因此反应停止后样品的质量不为0,所以图A所示的分析错误;
随着生铁不断与稀硫酸反应,放出氢气质量逐渐增大,至完全反应,放出氢气的质量=159.0g-158.7g=0.3g,所以图B的分析正确;
加入稀硫酸的质量=159.0g-44.1g-9.0g=105.9g,反应使溶液的质量逐渐增大,直到反应停止溶液质量不再改变,所以图C的分析错误;
故选:B;
②③设反应的铁的质量为x,生成的硫酸亚铁的质量为y
Fe+H2SO4═FeSO4+H2↑
56 152 2
x y 0.3g
$\frac{56}{x}$=$\frac{152}{y}$=$\frac{2}{0.3g}$
x=8.4g
y=22.8g
铁的质量分数为:$\frac{8.4g}{9g}$×100%=93.3%
硫酸亚铁的溶质质量分数为:$\frac{22.8g}{159g-9g-44.1g+8.4g-0.3g}$×100%=20%.
故答案为:①B;
②样品中铁的质量分数为93.3%;
③硫酸亚铁的溶质质量分数为20%.
点评 本题主要考查了化学方程式的计算,难度不大,注意解题的规范性和准确性.


 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案 期末集结号系列答案
期末集结号系列答案科目:初中化学 来源: 题型:解答题
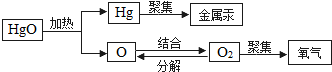 化学是在原子、分子水平上研究物质及其变化的科学.
化学是在原子、分子水平上研究物质及其变化的科学.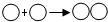 表示氧分子的形成过程
表示氧分子的形成过程查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | ②③ | B. | ②③④ | C. | ③④⑤ | D. | ①④⑤ |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
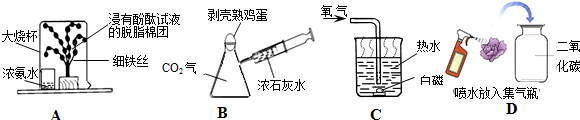
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
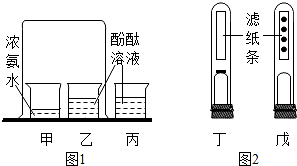
| A. | ①② | B. | ③④ | C. | ④⑤ | D. | ③⑤ |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 每个分子由4个碳原子、8个氢原子和2个氧原子构成 | |
| B. | 属于氧化物 | |
| C. | 碳、氢、氧三种元素质量比为6:1:4 | |
| D. | 相对分子质量为88 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com