
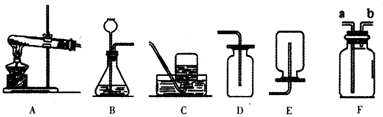
分析 ①根据实验室制取二氧化碳的反应是固体和液体,反应条件是常温,二氧化碳密度比空气大,易溶于水进行分析;
②根据使用长颈漏斗可以随时添加液体进行分析;
③根据长颈漏斗伸入液面以下的原因是防止生成的二氧化碳从长颈漏斗中逸出进行分析;
④根据二氧化碳的性质进行分析.
解答 解:①实验室制取二氧化碳的反应是固体和液体,反应条件是常温,所以发生装置是B,二氧化碳密度比空气大,易溶于水,所以收集装置是D;
②使用长颈漏斗可以随时添加液体;
③长颈漏斗伸入液面以下的原因是防止生成的二氧化碳从长颈漏斗中逸出;
④常用二氧化碳作灭火剂的原因是:二氧化碳密度比空气大,不助燃,不可燃.
故答案为:①B,D;
②随时添加液体;
③防止生成的二氧化碳从长颈漏斗中逸出;
④二氧化碳密度比空气大,不助燃,不可燃.
点评 本题主要考查常见气体的发生装置与收集装置的探究,发生装置依据反应物的状态和反应条件选择,收集装置依据气体的密度和溶解性选择.


科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
| 实验方案 | 实现现象 | 结论 |
| ①取一定量的合金粉末,加过量的30%的氢氧化钠溶液 ,充分反应后过滤,滤渣备用. | 粉末部分溶解,并有气体放出. | 合金中一定含有铝. |
| ②取步骤①所得滤渣,加过量的10%盐酸 ,充分反应. | 滤渣部分溶解,并有气体放出,溶液呈浅绿色. | 合金中一定含有铁和铜. |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 红磷在氧气中燃烧,产生大量白雾 | |
| B. | 木炭在氧气中剧烈燃烧,发白光,生成二氧化碳 | |
| C. | 硫在氧气中燃烧,发出蓝紫色火焰,生成无色无味气体 | |
| D. | 铁丝在氧气中燃烧,剧烈燃烧,火星四射,生成黑色固体 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 物质 | 杂质 | 除杂质应选用的试剂和操作方法 | |
| A | HCl气体 | CO2气体 | 先通过氢氧化钠溶液,再通过浓硫酸 |
| B | NaOH固体 | Na2CO3固体 | 加入过量盐酸,蒸发 |
| C | Cu(NO3)2溶液 | AgNO3溶液 | 加入过量的铜粉,过滤 |
| D | Fe | Cu | 加入适量的CuSO4溶液,过滤 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com