
分析 (1)依据质量守恒定律可以利用烧杯内物质的质量之差求出生成氢气的质量;
(2)根据氢气的质量利用方程式可以求出反应的锌的质量,从而可以求出弹壳中铜的质量;
(3)根据氢气的质量也可求出反应生成的硫酸锌的质量,进而求出所得溶液中ZnSO4的质量分数.
解答 解:(1)黄铜中的铜不能与酸反应生成氢气,而锌能与稀硫酸反应生成氢气,依据质量守恒定律可以利用烧杯内物质的质量之差求出生成氢气的质量为22g+100g-121.8g=0.2g;
(2)设反应的锌的质量是x,生成硫酸锌的质量是y
Zn+H2SO4=ZnSO4+H2↑
65 161 2
x y 0.2g
$\frac{65}{x}$=$\frac{161}{y}$=$\frac{2}{0.2g}$
x=6.5g,y=16.1g
弹壳中铜的质量:22g-6.5g=15.5g;
(3)反应后所得溶液中ZnSO4的质量分数:$\frac{16.1g}{121.8g-15.5g}$×100%=15.1%;
答:(1)产生氢气的质量是0.2g;
(2)弹壳中铜的质量是15.5g;
(3)反应后所得溶液中ZnSO4的质量分数15.1%.
点评 本题难度不是很大,利用质量守恒定律由反应前后烧杯内物质的总质量的差计算出生成氢气的质量是解答本题的突破口.


科目:初中化学 来源: 题型:解答题
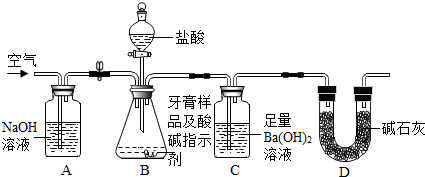
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 铝和稀盐酸 | B. | 氢氧化钠溶液和稀硫酸 | ||
| C. | KNO3溶液和BaCl2溶液 | D. | 氯化钠溶液和硝酸银溶液 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
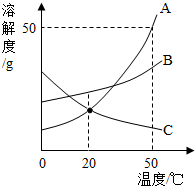
| A. | 50℃时,A物质饱和溶液中溶质的质量分数为50% | |
| B. | 将C的不饱和溶液变为饱和溶液,可采用增加溶质或降低温度的方法 | |
| C. | 将50℃时A、B、C三种物质的饱和溶液降温至20℃,C溶液中溶质质量分数最小 | |
| D. | A中混有少量的B,可用蒸发结晶法提纯 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
 位于香坊区的“中国亭园”已向游人开放.园内34座仿古名亭,都是按照1:1的比例复建的.当初这是原香坊、动力两区的垃圾倾卸场,常年堆积生活、工业、建筑垃圾,最高点距高压线仅为3.5米,累计囤积量约461万立方米.下列说法不正确的是( )
位于香坊区的“中国亭园”已向游人开放.园内34座仿古名亭,都是按照1:1的比例复建的.当初这是原香坊、动力两区的垃圾倾卸场,常年堆积生活、工业、建筑垃圾,最高点距高压线仅为3.5米,累计囤积量约461万立方米.下列说法不正确的是( )| A. | 将垃圾倾卸场改建成公园,这是一项造福百姓的工程 | |
| B. | 亭台楼阁的大理石地面主要成分是氧化钙 | |
| C. | 10余万株树木的栽种,增加了空气中的含氧量 | |
| D. | 园内50多个广场,为游人的歇息、休闲提供了方便 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
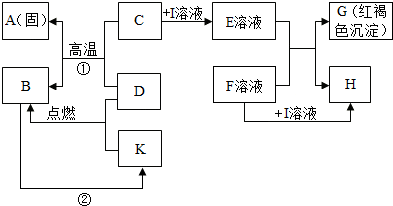
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 菠萝 pH=5.1 | B. | 草莓 pH=3.1 | C. | 苹果 pH=4.7 | D. | 柿子 pH=8.3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com