
·ÖĪö £Ø1£©øł¾Ż½šŹōµÄĪļĄķŠŌÖŹ½ųŠŠ·ÖĪö£»
£Ø2£©øł¾Ż¶žŃõ»ÆĢ¼ŗĶĒāŃõ»ÆøĘ·“Ӧɜ³ÉĢ¼ĖįøĘ³ĮµķŗĶĖ®½ųŠŠ·ÖĪö£»
£Ø3£©øł¾ŻĢ¼ĖįĒāÄĘŗĶŃĪĖį·“Ӧɜ³ÉĀČ»ÆÄĘ”¢Ė®ŗĶ¶žŃõ»ÆĢ¼½ųŠŠ·ÖĪö£»
£Ø4£©øł¾ŻÓ²Ė®ÖŠŗ¬ÓŠ½Ļ¶ąµÄæÉČÜŠŌøĘĆ¾»ÆŗĻĪļ£¬Ó²Ė®Čķ»ÆµÄ·½·ØÓŠÖó·Š”¢ÕōĮó½ųŠŠ·ÖĪö£®
½ā“š ½ā£ŗ£Ø1£©Ķ³£ÓĆÓŚÖĘ×÷µ¼Ļߣ¬Ö÷ŅŖĄūÓƵďĒĘäŃÓÕ¹ŠŌŗĶµ¼µēŠŌ£»
£Ø2£©¶žŃõ»ÆĢ¼ŗĶĒāŃõ»ÆøĘ·“Ӧɜ³ÉĢ¼ĖįøĘ³ĮµķŗĶĖ®£¬ĖłŅŌĒāŃõ»ÆøĘĪüŹÕ¶žŃõ»ÆĢ¼±ä³É¼į¹ĢµÄĢ¼ĖįøĘ£¬»Æѧ·½³ĢŹ½ĪŖ£ŗCa£ØOH£©2+CO2=CaCO3”ż+H2O£»
£Ø3£©Ģ¼ĖįĒāÄĘŗĶŃĪĖį·“Ӧɜ³ÉĀČ»ÆÄĘ”¢Ė®ŗĶ¶žŃõ»ÆĢ¼£¬»Æѧ·½³ĢŹ½ĪŖ£ŗNaHCO3+HCl=NaCl+H2O+CO2”ü£»
£Ø4£©Ó²Ė®ÖŠŗ¬ÓŠ½Ļ¶ąµÄæÉČÜŠŌøĘĆ¾»ÆŗĻĪļ£¬Ó²Ė®Čķ»ÆµÄ·½·ØÓŠÖó·Š”¢ÕōĮó£®
¹Ź“š°øĪŖ£ŗ£Ø1£©µ¼µē£»
£Ø2£©Ģ¼ĖįøĘ£¬Ca£ØOH£©2+CO2=CaCO3”ż+H2O£»
£Ø3£©NaHCO3+HCl=NaCl+H2O+CO2”ü£»
£Ø4£©Ca2+”¢Mg2+£¬Öó·Š”¢ÕōĮó£®
µćĘĄ ±¾Ģāæ¼²éµÄŹĒ³£¼ūµÄĪļÖŹµÄÓ¦ÓĆŅŌ¼°»Æѧ·½³ĢŹ½µÄŹéŠ“£¬Ķź³É“ĖĢā£¬æÉŅŌŅĄ¾ŻŅŃÓŠµÄĪļÖŹµÄŠŌÖŹŅŌ¼°»Æѧ·½³ĢŹ½µÄŹéŠ“·½·Ø½ųŠŠ£®


 ĆūŠ£æĪĢĆĻµĮŠ“š°ø
ĆūŠ£æĪĢĆĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | +1 | B£® | +2 | C£® | +3 | D£® | +4 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ²»ČÜĪļÖŠŅ»¶ØÓŠĶ | |
| B£® | ²»ČÜĪļÖŠæÉÄÜÓŠĢś | |
| C£® | ĀĖŅŗæÉÄÜŹĒĮņĖįĶ”¢ĮņĖįŃĒĢśµÄĮņĖįµÄ»ģŗĻČÜŅŗ | |
| D£® | ²»ČÜĪļµÄÖŹĮæ²»æÉÄÜÓėŌ»ģŗĻĪļÖŹĮæĻąµČ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ÓĆŹ³“׳żČ„ÅÆĖ®ĘæÖŠµÄ±”²ćĖ®¹ø | |
| B£® | ÓĆ×ĘÉÕ²¢ĪÅĘųĪ¶µÄ·½·ØĒų±š“æĆŽÖÆĪļŗĶ“æĆ«ÖÆĪļ | |
| C£® | ÓĆŹ³ÓĆ¼ī£ØNa2CO3£©ČÜŅŗĻ“µÓ²Ķ¾ßÉĻµÄÓĶĪŪ | |
| D£® | ÓĆĆ×ĢĄ¼ģŃéµāĖį¼Ų£ØKIO3£© |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¼ÓŃ¹Ź±25Į¢·½Ć׵ďÆÓĶĘųæÉ×°ČėĢå»żĪŖ0.024Į¢·½Ć×µÄøÖĘæÖŠ--·Ö×ÓŌŚ²»Ķ£µÄŌĖ¶Æ | |
| B£® | ½µµĶĪĀ¶ČŹ±Ä³ČÜŅŗÖŠÓŠ¾§ĢåĪö³ö--øĆČÜŅŗ½µĪĀĒ°Ņ»¶ØŹĒ±„ŗĶČÜŅŗ | |
| C£® | ³£ĪĀŹ±Ä³ČÜŅŗÄÜŹ¹·ÓĢŖČÜŅŗ±äŗģ--øĆČÜŅŗŅ»¶ØŹĒ¼īµÄČÜŅŗ | |
| D£® | ijĪļÖŹŌŚæÕĘųÖŠČ¼ÉÕŗóÉś³É¶žŃõ»ÆĢ¼ŗĶĖ®--øĆĪļÖŹÖŠŅ»¶Øŗ¬ÓŠC”¢HŌŖĖŲ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 ĻĀĶ¼±ķŹ¾µē½āĖ®µÄ¼ņŅ××°ÖĆ£®»Ų“šĻĀĮŠĪŹĢā£ŗ
ĻĀĶ¼±ķŹ¾µē½āĖ®µÄ¼ņŅ××°ÖĆ£®»Ų“šĻĀĮŠĪŹĢā£ŗ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢ½¾æĢā
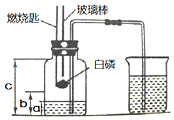 ijæĘѧŠĖȤŠ”×éµÄĶ¬Ń§ŌŚŃ§Ļ°ĮĖæÕĘųÖŠŃõĘųŗ¬ĮæµÄ²ā¶ØµÄ»ł“”ÉĻ£¬øĽųĮĖ½Ģ²ÄÖŠµÄŹµŃ飬Éč¼Ę³öĮĖČēĶ¼ĖłŹ¾µÄŹµŃé×°ÖĆ£®ŹµŃé²½ÖčČēĻĀ£ŗ
ijæĘѧŠĖȤŠ”×éµÄĶ¬Ń§ŌŚŃ§Ļ°ĮĖæÕĘųÖŠŃõĘųŗ¬ĮæµÄ²ā¶ØµÄ»ł“”ÉĻ£¬øĽųĮĖ½Ģ²ÄÖŠµÄŹµŃ飬Éč¼Ę³öĮĖČēĶ¼ĖłŹ¾µÄŹµŃé×°ÖĆ£®ŹµŃé²½ÖčČēĻĀ£ŗ²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com