
分析 (1)由生成氢气的质量,由反应的化学方程式列式计算出生成氧气的质量即可.
(2)根据溶液电解前后溶质的质量不变,结合题意进行分析解答.
解答 解:(1)设生成氧气的质量为x
2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑
4 32
2g x
$\frac{4}{32}=\frac{2g}{x}$ x=16g
(2)由质量守恒定律,参加反应的水的质量为2g+16g=18g.
溶液电解前后溶质的质量不变,实验后所得氢氧化钠溶液的溶质质量分数为$\frac{2g}{2g+50g-18g}$×100%≈5.9%.
答:(1)生成氧气的质量为16g;(2)实验后所得氢氧化钠溶液的溶质质量分数为5.9%.
点评 本题难度不大,掌握利用化学方程式的简单计算、溶质质量分数的计算并能灵活运用是正确解答本题的关键.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
 在如图所示的装置中进行空气成分的探究实验.已知当温度达到200℃磷就能在空气中燃烧.在实验开始时先将弹簧夹夹住橡皮导气管,然后设法点燃红磷,在红磷燃烧停止并等到烧瓶冷却再打开弹簧夹.试回答下列问题:
在如图所示的装置中进行空气成分的探究实验.已知当温度达到200℃磷就能在空气中燃烧.在实验开始时先将弹簧夹夹住橡皮导气管,然后设法点燃红磷,在红磷燃烧停止并等到烧瓶冷却再打开弹簧夹.试回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
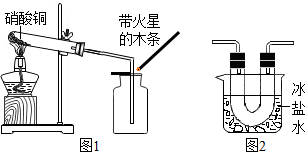 硝酸铜为蓝色固体,水溶液为蓝色,某小组用图1装置加热硝酸铜,观察到固体由蓝色逐渐变黑,产生红棕色气体,带火星的木条复燃.
硝酸铜为蓝色固体,水溶液为蓝色,某小组用图1装置加热硝酸铜,观察到固体由蓝色逐渐变黑,产生红棕色气体,带火星的木条复燃.查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
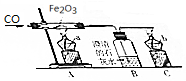 如图是炼铁的原理图
如图是炼铁的原理图查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com