
【题目】能源“非石油化”是战略目标,发展以CH4、CO2等为原料的“C1化学”成为化工生产的必然趋势。通常天然气中含有H2S等有毒气体,图为天然气合成氨的工艺流程。下列说法正确的是
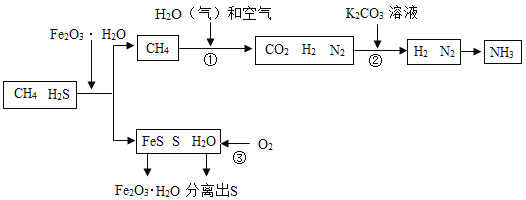
A.N2、H2按照质量比1:3合成氨气
B.用Fe2O3.H2O除去H2S,生成物中含硫元素的物质有1种
C.该流程中可参与循环的物质有Fe2O3·H2O
D.反应①中主要发生的化学反应方程式(反应条件略去):![]()
科目:初中化学 来源: 题型:
【题目】t1℃时,取a、b两种固体物质各25g于两只烧杯中,分别加入100g水,充分溶解后,两种固体均有剩余。升温到t2℃时,a完全溶解,b固体增多。a、b两种物质的溶解度曲线如图所示。以下判断正确的是( )
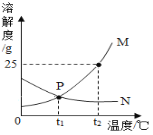
A. 图中曲线M表示b物质的溶解度曲线
B. t1℃时,两只烧杯中剩余物质的质量不相等
C. t2℃时,两只烧杯中的溶液都是饱和溶液
D. t2℃时,两只烧杯中溶液的溶质质量分数相同
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】小明利用图 1 装置探究物质在空气中燃烧后氧气浓度变化(已知:白磷的着火点是40℃,红磷的着火点是240℃)。图 2 是用传感器测量整个实验过程中烧瓶内氧气浓度变化情况的曲线。
步骤 1:用激光笔照射燃烧匙中足量的红磷,红磷燃烧,一段时间后熄灭;白磷始终不燃烧。
步骤 2:冷却至室温,将装有白磷的燃烧匙提岀水面,用激光笔照射,白磷燃烧。
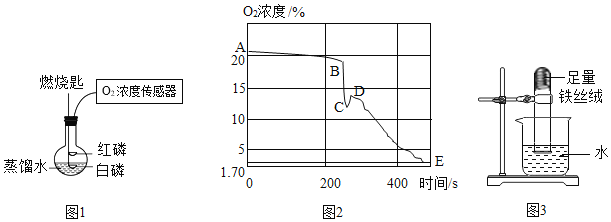
(1)在步骤 1 开始前应进行的操作是__________________;步骤 1 中激光笔的作用是________________;
(2)在步骤 1 中反应的化学方程式为___________________;图 2 表示红磷燃烧的曲线是_____________;该曲线对应装置内压强变化情况是______________;
(3)你认为“测定空气中氧气的含量”,选择______________(填“红磷”或“白磷”)效果会更好;
(4)通过本实验你对物质的燃烧有什么新的认识?________________;
(5)图 2 中 CD 段氧气浓度变化的主要原因是:________________;DE 段氧气浓度变化的主要原因是:____________________;
(6)查阅资料可知,测定空气中氧气含量较好的药品是铁丝绒,利用的原理是铁与氧气、水发生缓慢氧化而生锈,用图 3 所示装置完成实验,最终观察到的现象是____________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图“黑面包”实验中,蔗糖(C12H22O11)变黑,体积膨胀,变成疏松的炭,放出有刺激性气味的气体。
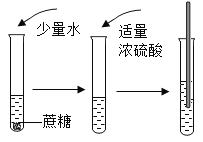
(提出问题)改变糖的种类、浓硫酸的体积、水的滴数和温度是否会影响实验效果呢?
(进行实验)分别取5g糖粉进行实验,根据前2 min的现象对实验效果进行评分,记录如下:
表1 实验记录
实验 | 糖 | 浓硫酸体积/mL | 水的滴数 | 温度/℃ | 效果得分 |
1 | 蔗糖 | 4 | 5 | 22 | 65 |
2 | 蔗糖 | 5 | 10 | 30 | 81 |
3 | 蔗糖 | 6 | 15 | 50 | 93 |
4 | 冰糖 | 4 | 10 | 50 | 91 |
5 | 冰糖 | 5 | 15 | 22 | 88 |
6 | 冰糖 | a | 5 | 30 | 75 |
7 | 葡萄糖 | 4 | 15 | 30 | 0 |
8 | 葡萄糖 | 5 | 5 | 50 | 0 |
9 | 葡萄糖 | 6 | 10 | 22 | 0 |
(处理数据)分析表1,计算效果得分均值,结果如下:
表2 效果得分均值
因素 | 糖 | 浓硫酸体积/mL | 水的滴数 | 温度/℃ | ||||||||
蔗糖 | 冰糖 | 葡萄糖 | 4 | 5 | 6 | 5 | 10 | 15 | 22 | 30 | 50 | |
均值 | 79.7 | 84.7 | 0 | 52.0 | 56.3 | 56.0 | 46.7 | 57.3 | 60.3 | 51.0 | 52.0 | 61.3 |
依据均值推断最佳实验方案,均值越高,效果越好。
(解释与结论)
(1)推测放出的气体含SO2,从元素守恒角度说明理由_____;
(2)实验6中,a为_____mL;
(3)根据表2推断,“黑面包”实验最好选择5 g冰糖、5 mL浓硫酸、_____滴水和50 ℃;
(反思与评价)
(4)表2中,22 ℃对应的均值为51.0,计算该值所依据的3个数据分别是_____;
(5)综合分析,使实验3的效果得分高于实验4的因素有_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】铁及其化合物的有关知识
(一)铁及其化合物的应用
1如图1为某小儿硫酸亚铁糖浆。适当服用该糖浆可治疗_____(选填序号)。
A佝偻病
B侏儒症
C贫血症
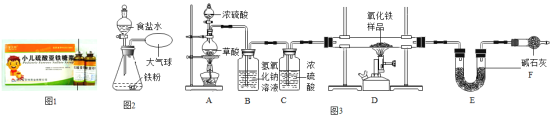
2食品保鲜“双吸剂”含铁粉、食盐等,如图2为其原理探究实验: 滴入食盐水后,关闭分液漏斗活塞。一段时间后,铁粉上出现红色固体,气球_______(选填“变大”、“不变”或“变小”)。食盐水的作用是_______。
(二)铁及其化合物的实验
某化学兴趣小组在实验室中模拟工业炼铁的原理,并探究CO与Fe2O3反应后的产物。
[查阅资料]:
草酸(H2C2O4) 固体与浓硫酸混合加热会产生一氧化碳,反应方程式为:
②NaOH溶液可以吸收二氧化碳,浓硫酸是一种常用的干燥剂,碱石灰既能吸收二氧化碳也能吸水。于是他设计了如图3的实验装置,结合装置回答下列问题:
1图中装置C作用是______;
2从实验操作程序和实验安全看,首先要检查装置的气密性,实验开始先加热_______(填A或D)处。
3该装置设计有一个明显缺陷,你认为是_______。
4将Fe粉溶于稀H2SO4,用点燃法检验生成的H2前必须_____。向反应后的溶液中滴加NaOH溶液,生成白色Fe(OH)2沉淀,随后沉淀变为灰绿色。白色沉淀变为灰绿色的原因之一是部分Fe(OH)2接触空气生成Fe(OH)3,反应的化学方程式_____。生成的Fe(OH)3分解为Fe2O3。过滤、洗涤、低温干燥得到灰绿色固体,其组成为2FeSO4·2Fe(OH)2·Fe2O3[相对分子质量为644]。
(三)灰绿色固体的热分解实验
兴趣小组称取此固体6.44g,在科研人员的指导下用下图装置进行热分解实验。
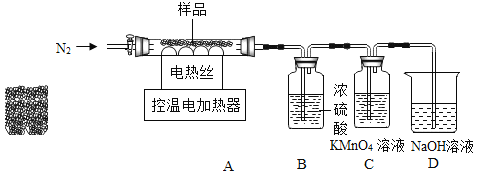
[查阅资料]①Fe(OH)2在150℃~200℃时完全分解为FeO;
②FeSO4在450℃~ 500℃时完全分解为Fe2O3,
![]()
1加热前后及过程中均通入N2,加热结束后仍通一段时间N2的目的是________。
2控制温度在不同的范围对A中样品加热。测得剩余固体质量随温度的变化如图所示。B装置中浓硫酸只能吸收SO3和H2O,当加热到t1℃时,装置C中的现象为______。
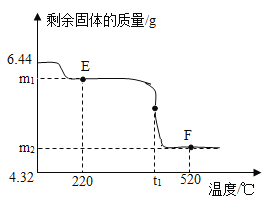
①图中E点对应的m1=_____。
②图中F点对应物质中Fe2O3的质量为___g。
③科研人员将F点所得剩余固体隔绝空气,在密闭容器中加热到1400℃,已知加热过程中发生反应,且反应前后固体总质量不变,得到纯净的化合物。请写出该化合物的化学式______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某实验小组为探究酸的化学性质,由甲、乙同学设计并完成了如图所示的实验。

(查阅资料)CaCl2、NaCl 的溶液呈中性;
(实验探究一)确定甲、乙同学上述实验后所得溶液中的溶质。
(1)取甲所得溶液少许,加入石蕊试液,溶液显红色,甲所得溶液中一定含有的溶质是_____(写化学式)。
(2)取乙所得溶液少许,加入酚酞试液,溶液显红色,乙所得溶液中一定含有的溶质是_____(写化学式)。
(实验探究二)确定甲、乙同学上述实验所得溶液混合后的成分。甲、乙同学把上述实验所得溶液倒入同一废液缸中,观察到先有气泡产生,后有白色沉淀生成,同学们将烧杯内的物质进行过滤,对所得滤液的溶质成分进行探究。
(提出猜想)
A 同学猜想 NaCl、Na2CO3
B 同学猜想:NaCl、CaCl2
C 同学猜想:NaCl、CaCl2、HCl
你的猜想:_____。
(交流讨论)你认为_____同学的猜想一定不正确。
(设计实验)请设计实验证明 A 的猜想正确。
实验步骤 | 实验现象 | 实验结论 |
取少量滤液于试管中,向其中滴加_____。 | _____。 | 猜想成立。 |
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图是制取饮用水消毒剂二氧化氯的微观过程图。下列说法错误的是
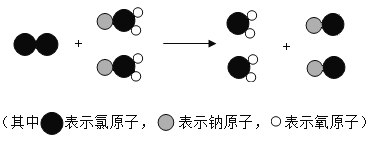
A.二氧化氯的化学式为ClO2
B.二氧化氯中氯元素的化合价为+4
C.反应物和生成物中共有两种氧化物
D.化学反应前后原子的种类不变
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】用所学知识回答。
(1)实验室常用的燃料是______,写出它完全燃烧的化学方程式__________。
(2)高压水枪灭火所依据的灭火原理是__________________。
(3)用微粒观点解释:香水要密封保存___________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com