
| A. | 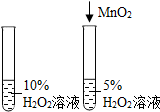 探究MnO2对 探究MnO2对反应速率的影响 | B. | 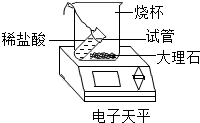 验证化学反应前后质量守恒 验证化学反应前后质量守恒 | ||
| C. | 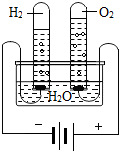 测定水的 测定水的组成 | D. | 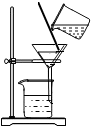 除去氯化钠溶液中混有的硝酸钾 除去氯化钠溶液中混有的硝酸钾 |
分析 A、根据对照试验的设计方法考虑;
B、根据碳酸钙和盐酸反应会生成二氧化碳进行分析;
C、根据产物结合质量守恒定律进行分析;
D、根据过滤的原理分析.
解答 解:A、对照试验,一个放二氧化锰,一个不放二氧化锰,但过氧化氢溶液浓度不同,所以不能达到实验目的,故错误;
B、碳酸钙和盐酸反应会生成二氧化碳,验证质量守恒定律应该在密闭容器内进行实验,故错误;
C、电解水是产生氧气和氢气,生成的氢气是由氢元素组成的,氧气是由氧元素组成的,由质量守恒定律,反应前后元素种类不变,则该实验证明水是由氢、氧两种元素组成的;故正确;
D、氯化钠、硝酸钾均易溶于水,不能用过滤的方法除去氯化钠溶液中的硝酸钾;故错误;
故选项为:C.
点评 本题是有关实验方案的设计和评价的考查,要求学生熟悉所实验的内容及原理,完成此题,可以依据已有的知识进行.


科目:初中化学 来源: 题型:解答题
 有“中国死海”之称的山西运城盐湖中主要含两种盐Ma2SO4和NaCl,这两种物质的溶解度如下表所示:
有“中国死海”之称的山西运城盐湖中主要含两种盐Ma2SO4和NaCl,这两种物质的溶解度如下表所示:| 温度/℃ 溶解度/g | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 |
| Ma2SO4 | 4.9 | 9.1 | 19.5 | 40.8 | 48.8 | 46.2 | 45.3 | 44.3 |
| NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 | 37.8 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 高铁酸钠属于有机化合物 | |
| B. | 高铁酸钠由钠、铁、氧三种元素组成 | |
| C. | 高铁酸钠中钠、碳、氧三种元素的原子个数比为2:1:4 | |
| D. | 高铁酸钠中钠元素的质量分数最小 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:多选题
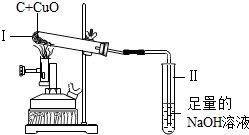 一定量的碳与氧化铜混合加热,反应前后测定装置I、Ⅱ的质量如下.分析错误的是( )
一定量的碳与氧化铜混合加热,反应前后测定装置I、Ⅱ的质量如下.分析错误的是( )| 反应前质量(g) | 反应后质量(g) | |
| 装置I | 56.3 | 55.2 |
| 装置II | 242.9 | 243.7 |
| A. | 生成的气体是混合物 | |
| B. | I中减少的质量是氧元素的质量 | |
| C. | 反应后I中固体成分可能有3种情况 | |
| D. | Ⅱ中增加的质量是吸收的二氧化碳的质量 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
| 脱氧剂 | 洁厕灵 | 炉灶清洁剂 | |
| 有效成分 | 还原铁粉 | 盐酸 | 氢氧化钠(分解油污,有强烈的腐蚀性) |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com