
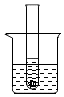
 如图所示,在盛有冷水的烧杯中放着一支试管,试管中是饱和的氯化钠溶液和部分未溶的氯化钠固体.现向烧杯中的水中加入适量的氢氧化钠固体,再恢复到原来的温度,下列各相关的变化图象正确的是( )
如图所示,在盛有冷水的烧杯中放着一支试管,试管中是饱和的氯化钠溶液和部分未溶的氯化钠固体.现向烧杯中的水中加入适量的氢氧化钠固体,再恢复到原来的温度,下列各相关的变化图象正确的是( )| A. |  | B. | 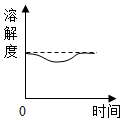 | C. |  | D. |  |
分析 根据氯化钠的溶解度随温度的升高而增大,氢氧化钠固体溶于水放出热量,在盛有冷水的烧杯中放着一支试管,试管中是饱和的氯化钠溶液和部分未溶的氯化钠固体,现向烧杯中的水中加入适量的氢氧化钠固体,再恢复到原来的温度,氯化钠的溶解度会先增大,然后恢复到原来的数值,然后结合题中的选项进行分析.
解答 解:氯化钠的溶解度随温度的升高而增大,氢氧化钠固体溶于水放出热量,在盛有冷水的烧杯中放着一支试管,试管中是饱和的氯化钠溶液和部分未溶的氯化钠固体,现向烧杯中的水中加入适量的氢氧化钠固体,再恢复到原来的温度,氯化钠的溶解度会先增大,然后恢复到原来的数值,所以
A、溶液的质量会逐渐的增大,恢复到原来的温度时,溶液的质量也会恢复到原来的状态,故A错误;
B、溶液温度升高,溶解度会逐渐增大,恢复到原来的温度时,溶解度也会减小到原来的数值,故B错误;
C、温度改变前后,溶剂的质量不变,故C正确;
D、恢复到原来的温度时,溶质质量分数只会恢复到原来的状态,故D错误.
故选:C.
点评 本题主要考查了温度变化对饱和溶液中一些数据的影响,难度不大,认真分析题意即可解答.


科目:初中化学 来源: 题型:解答题
| 元素 | O | Mg | Al | Cl |
| 原子结构 示意图 |  | 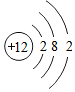 | 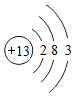 | 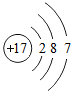 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | Cu>R>Mg | B. | Mg>R>Cu | C. | R>Mg>Cu | D. | Mg>Cu>R |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 序号 | ① | ② | ③ | ④ |
| 物质 | 醋酸 | 高锰酸钾 | 消石灰 | 纯碱 |
| 化学式 | CH3COOH | KMnO4 | Ca(OH)2 | Na2CO3 |
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 吸入的气体比呼出的气体氧气含量大 | |
| B. | 吸入的气体比呼出的气体二氧化碳含量大 | |
| C. | 吸入的气体比呼出的气体水蒸气含量大 | |
| D. | 吸入的气体和呼出的气体氮气含量几乎没有变化 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | $\frac{1}{3}$ | B. | $\frac{1}{4}$ | C. | $\frac{1}{2}$ | D. | $\frac{2}{3}$ |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
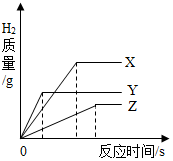 把相同体积、相同质量分数的足量稀盐酸,分别滴加到等质量、颗粒大小相同的X、Y、Z三种较活泼的金属中,生成H2的质量与反应时间的关系如图所示.这三种金属的活动性顺序为Y>X>Z;假如X、Y、Z都是+2价金属,则相对原子质量由大到小的顺序为Z>Y>X
把相同体积、相同质量分数的足量稀盐酸,分别滴加到等质量、颗粒大小相同的X、Y、Z三种较活泼的金属中,生成H2的质量与反应时间的关系如图所示.这三种金属的活动性顺序为Y>X>Z;假如X、Y、Z都是+2价金属,则相对原子质量由大到小的顺序为Z>Y>X查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com