
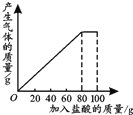
 有一种石灰石样品的成分是CaCO3和SiO2.课外小组同学将100g盐酸分5次加入到35g石灰石样品中(已知SiO2不与盐酸反应),得到如下部分数据和图象.
有一种石灰石样品的成分是CaCO3和SiO2.课外小组同学将100g盐酸分5次加入到35g石灰石样品中(已知SiO2不与盐酸反应),得到如下部分数据和图象. | 次数 | 第1次 | 第2次 | 第3次 |
| 加入盐酸的质量/g | 20 | 20 | 20 |
| 剩余固体的质量/g | 30 | a | 20 |
分析 (1)由图表分析,三次参加反应的物质质量相等,由此计算出第二次参加反应的物质质量,再由剩余固体的质量=总质量-参加反应的物质质量可计算出a的值;
(2)根据题意和图表分析,可得到样品中CaCO3的质量,再根据CaCO3中钙元素、碳元素和氧元素的质量计算出它们各占的比值;
(3)4次反应固体物质减少的质量即为样品中碳酸钙的质量,据此计算样品中碳酸钙质量分数;
根据碳酸钙与盐酸反应的方程式,由二氧化碳的质量可以求出碳酸钙的质量,再求出石灰石样品的质量.
解答 解:(1)由图象可知,第四次加入盐酸后,才得到完全反应,故在反应过程中,第一次充分反应后剩余固体的质量为30g,说明只有35g-30g=5g样品参与了反应,第三次充分反应后剩余固体的质量为20g,说明共有35g-20g=15g样品参与了反应,故第二次充分反应时,也只有5g样品参与了反应,故第2次加入盐酸后,a=35g-5g×2=25g;
故答案为25.
(2)根据图象分析,第4次加入盐酸后,样品中CaCO3完全反应.
样品中钙元素、碳元素和氧元素的质量比:
(20g×$\frac{40}{100}$):(20g×$\frac{12}{100}$):(20g×$\frac{48}{100}$+15g×$\frac{32}{60}$)=10:3:22
答:石灰石样品中钙元素、碳元素和氧元素的质量比为10:3:22.
(3)(2)第4次加入稀盐酸后,固体物质总共减少的质量=5g×4=20g,
则石灰石样品中碳酸钙的质量分数$\frac{20g}{35g}$×100%≈57.1%
解:设需CaCO3的质量为x.
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 44
x 4.4g
$\frac{100}{x}=\frac{44}{4.4g}$
解得 x=10g
需石灰石样品的质量为$\frac{10g}{57.1%}$=17.5g.
点评 本题要求学生了解完全反应和不完全反应的概念及特点,观察图表,分析数据,正确解答.在计算石灰石样品中钙元素、碳元素和氧元素的质量比为时,一定注意氧元素不只碳酸钙中有,二氧化硅中也有氧元素.


科目:初中化学 来源: 题型:选择题
| 物质 | 乙醇 | 氧气 | 二氧化碳 | 水 | X |
| 反应前质量g | 4.6 | 8 | 0 | 0 | 0 |
| 反应后质量g | 0 | 0 | 4.4 | 5.4 | m |
| A. | 表中m的值为2.8 | B. | X是该反应的催化剂 | ||
| C. | 物质X中含有氧元素 | D. | 物质X中含有碳元素 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验步骤 | 实验现象 | 实验结论 | |
| 实验一 | ① | 木条不复燃 | 常温下过氧化氢溶液不分解 |
| 实验二 | 在装有过氧化氢溶液的试管中加入水泥块,然后将带火星的小木条伸入试管中 | 木条复燃 | ② 加入水泥块能加快过氧化氢的分解速率 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 若向滤渣A中滴加稀盐酸有气泡生成,则滤渣A中一定含有Ag | |
| B. | 若向滤渣A中滴加稀盐酸无气泡生成,则滤液B中可能含有Cu2+ | |
| C. | 若向滤液B中滴加稀盐酸产生白色沉淀,则滤液B中可能含有Fe2+ | |
| D. | 若向滤液B中滴加稀盐酸无明显变化,则滤渣A中一定含有Ag,可能含有Cu |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
 Ⅰ、水与人类的生活和生产密切相关,请回答以下问题:
Ⅰ、水与人类的生活和生产密切相关,请回答以下问题:| 项目 地点 | A | B | C |
| pH | 6 | 4 | 5 |
| 1L水中溶解的氧气 | 0.011g | 0.007g | 0.003g |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com