
| +2 |
| Mg |
| +2 |
| Mg |
| +2 |
| Mg |
| +2 |
| Mg |


 英才点津系列答案
英才点津系列答案 红果子三级测试卷系列答案
红果子三级测试卷系列答案科目:初中化学 来源: 题型:


查看答案和解析>>
科目:初中化学 来源: 题型:
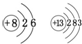
 (3)上表中硫元素的每个原子需要得到
(3)上表中硫元素的每个原子需要得到查看答案和解析>>
科目:初中化学 来源: 题型:




查看答案和解析>>
科目:初中化学 来源: 题型:

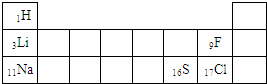
 下表是元素周期表的一部分(数字表示相应元素的原子序数),请用元素符号将两种元素填入表中相应位置.
下表是元素周期表的一部分(数字表示相应元素的原子序数),请用元素符号将两种元素填入表中相应位置.
| 1H | 2He | ||||||
| 3Li | 4Be | 5B | 9F | 10Ne | |||
| 11Na | 14Si | 16S | 17Cl | 18Ar | |||
查看答案和解析>>
科目:初中化学 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com