
【题目】某学校研究小组为了测定当地石灰石中碳酸钙的质量分数(石灰石中的杂质既不溶于水,也不与酸反应), 取来了一些矿石样品,并取稀盐酸400g,平均分成4份,进行分组实验,,结果如下:
实验分组 | 一 | 二 | 三 | 四 |
加入矿石样品的质量/g | 10 | 20 | 30 | 40 |
生成二氧化碳的质量/g | 3.52 | 7.04 | 8.8 | m |
试回答并计算:
(1)表中m的数值为_____________________。
(2)这种石灰石中碳酸钙的质量分数是多少___________?
(3)所用稀盐酸的溶质质量分数是多少___________?
 能力评价系列答案
能力评价系列答案 唐印文化课时测评系列答案
唐印文化课时测评系列答案 导学与测试系列答案
导学与测试系列答案科目:初中化学 来源: 题型:
【题目】如图是三种物质的溶解度曲线,下列说法正确的是( )
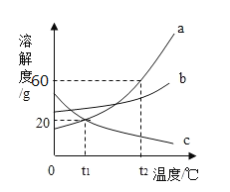
A. 物质c的溶解度随温度的升高而增大
B. 物质a的溶解度大于物质c的溶解度
C. t2℃时,60g物质a与100g水充分混合后所得溶液的总质量为160g
D. 将t1℃时,b、c两种物质的饱和溶液升温至t2℃,溶液中溶质质量分数均不变
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】自然界中二氧化碳的循环下列五幅图片是二氧化碳在大气圈和水圈循环的示意图,图中的数据表示二氧化碳的相对量,没有具体单位.请你仔细分析图示,结合已有知识回答下列问题:

(1)将五幅图中所有吸收二氧化碳的相对量总和与所有释放二氧化碳的相对量总和比较,你的发现是_____.
(2)图(Ⅰ)所示土壤中释放出二氧化碳的途径中包括:土壤中的碳酸盐与酸(盐酸)作用:土壤中的碳酸盐受热分解,请你各举一例,写出化学方程式:_____、_____.
(3)图(Ⅴ)中植物吸收和释放二氧化碳相对量相差较大的主要原因是:_____.
(4)能源是社会发展的基础.化石燃料是目前人类最重要的能源物质,请回答:
①下列燃料中,属于化石燃料的是_____(填字母符号)
A汽油 B液化石油气 C柴油 D木炭 E天然气 F焦炭 G柴草 H酒精
②煤燃烧的产物有二氧化碳、二氧化硫、二氧化氮和水等,由此你认为煤中一定含有_____元素,推断的依据是_____.
③化石燃料加工主要有以下几种方法,其中主要发生化学变化的是_____(填字母编号).
A石油的裂解 B石油的分馏 C煤的焦化 D煤的气化 E煤的液化
④汽油是石油分馏所得的产物之一,其成分之一为C7H16,写出该物质完全燃烧的化学方程式_____.
(5)为减少空气污染和温室气体排放,经研究发现不含碳元素的NH3燃烧产物没有污染,且释放大量能量,请写出NH3燃烧的化学方程式_____.
(6)燃烧是一类重要的化学反应,对于燃烧的下列认识正确的是_____(填字母序号)
A通常所说的燃烧是可燃物跟氧气发生的剧烈的发光、发热的氧化反应
B通过控制温度(着火点以上或以下)可以使可燃物与氧气的燃烧反应发生或停止
C在燃烧过程中,可燃物中储存的能量以光能或热能的形式释放出来
D在人类社会的发展进程中燃烧利大于弊
E物质发生燃烧时都会产生火焰.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】已知某物质在20℃ 和40℃ 时的溶解度分别为10g和40g。某温下,将5g该物质加到20g水中,下列有关叙述正确的是
A. 20℃ 时,所得溶液的质量为25g
B. 40℃ 时,所得溶液为饱和溶液
C. 不管什么温度下,所得溶液的溶质质量分数均为20%
D. 该物质的溶解度随温度的升高而增大
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据图中提供的信息,请回答下列问题:
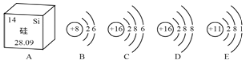
(1)B、C、D、E表示的粒子中化学性质相似的是______(填字母序号);
(2)由A 图信息可推知,硅位于元素周期表的第_______周期
(3)与D图表示的粒子电子层排列相同的原子是__________(填化学符号);
(4)C、E两种元素组成化合物的化学式为___________.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】碲(Te)被誉为“现代工业、国防与尖端技术的维生素,创造人间奇迹的桥梁”。实验室模拟提取碲的一个实验是:取某含碲溶液于烧瓶中,加入适量NaCl,加热到一定温度,持续通入SO2,待反应一段时间,过滤得到粗碲。
(1)反应的总化学方程式为: ![]() ,则X为______(填化学式);
,则X为______(填化学式);
(2)为探究获得较高粗碲沉淀率的反应条件,某研究小组在控制NaCl浓度和SO2流量不变的条件下,进行下述对比试验,数据如下:
实验 | 温度/℃ | 反应时间/h | 粗碲沉淀率/% |
a | 65 | 3.0 | 65.0 |
b | 80 | 3.0 | 98.9 |
c | 80 | 2.0 | 98.9 |
d | 90 | 2.0 | 97.0 |
①该小组研究的反应条件是______和______;
②实验a和b 的目的是______;
③为了提升设备利用效率和节约能源,可进一步优化反应条件测定粗碲沉淀率。若再设计对比实验,选择的反应条件还可以是______(填序号)。
A 80℃,1.5h B 80℃,2.5h C 70℃,2.0h D 95℃, 2.0h
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】元素周期表是学习和研究化学的重要工具.A、B、C为周期表1﹣18号中的元素,在周期表中的位置如图所示.已知A元素的单质是空气的主要成分之一,三种元素的核电荷数之和为31.
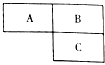
(1)A元素的名称为:____;
(2)B元素单质的一种用途为____;
(3)C的单质与氧气反应的化学方程式为_____;
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】现有盐酸和氯化镁的混合溶液,向其中逐滴滴入氢氧化钠溶液,生成沉淀质量与滴入氢氧化钠溶液质量的变化关系如图所示。下列说法错误的是
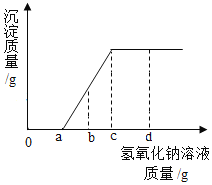
A. 滴加氢氧化钠溶液质量为a~cg时,溶液中发生的反应为:![]()
B. 滴加氢氧化钠溶液质量至ag时,溶液中溶质质量比原混合溶液中溶质质量大
C. 滴加氢氧化钠溶液质量至bg时,溶液中含三种溶质
D. 滴加氢氧化溶液质量至cg时,溶液呈中性
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】溶液与人们的生产、生活密切相关。
图1为甲、乙两种固体物质的溶解度曲线。
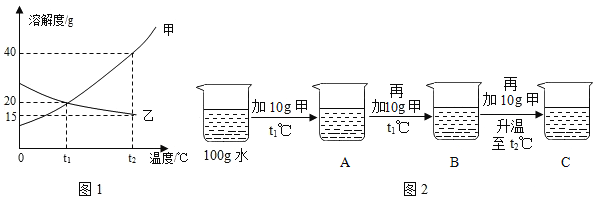
(1)溶解度随温度升高而增大的物质是_____ (填“甲”或“乙”)。
(2)某同学按图2所示进行实验,得到相应温度下的A、B、C三种溶液,在A、B、C三种溶液中属于饱和溶液的是_____(填字母)。 向C中再加入25g 甲,充分搅拌,恢复到t2℃时,所得溶液中溶质的质量分数为_____(结果精确到0.1%)。
(3)将t2℃时的甲、乙两种物质的饱和溶液降温至t1℃,所得溶液中溶质的质量分数:甲_____乙(填“<”“=”或“>”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com