
【题目】下列化学方程式符合题意且书写和所属基本反应类型均正确的是( )
A. 不能用铁器盛放硫酸铜溶液的原因:Fe+CuSO4=FeSO4+Cu 置换反应
B. 铝耐腐蚀的原因:4Al+3O2=Al2O3 氧化反应
C. 工业上以赤铁矿为原料冶炼生铁:2Fe2O3+3C![]() 4Fe+ 3CO2↑ 还原反应
4Fe+ 3CO2↑ 还原反应
D. 电解水产生氢气和氧气:2H2O![]() 2H2↑+ O2 ↑ 分解反应
2H2↑+ O2 ↑ 分解反应
【答案】A
【解析】
根据化学方程式判断正误的方法需考虑:应用的原理是否正确;化学式书写是否正确;是否配平;反应条件是否正确;↑和↓的标注是否正确;若化学方程式正确,再判断反应类型是否正确。
A、该化学方程式书写完全正确,且该反应是一种单质和一种化合物反应生成另一种单质和另一种化合物的反应,属于置换反应,故A选项正确。
B、该化学方程式配平错误,正确的化学方程式应为![]() ,且氧化反应不是基本的反应类型,故B选项错误。
,且氧化反应不是基本的反应类型,故B选项错误。
C、工业上用一氧化碳还原氧化铁炼铁,主要是利用CO的还原性,在高温下和氧化铁反应生成铁和二氧化碳,正确的化学方程式为![]() ,且还原反应不是基本反应类型,故C选项错误。
,且还原反应不是基本反应类型,故C选项错误。
D、该化学方程式的反应条件应为通电,正确的化学方程式应为![]() ,故D选项错误。
,故D选项错误。
故选:A。


科目:初中化学 来源: 题型:
【题目】我国科学家屠哟哟因发现青蒿素(化学式![]() )而获得诺贝尔奖。下列有关青蒿素的说法错误的是
)而获得诺贝尔奖。下列有关青蒿素的说法错误的是
A. 属于化合物
B. 碳元素的质量分数最高
C. 一个分子中含有42个原子
D. 分子中C、H、O三种原子质量比为15:22:5
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验室用来制备和收集气体的部分装置如图所示:
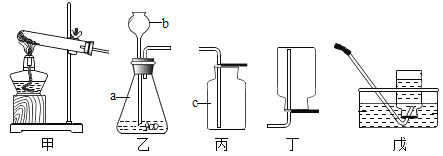
(1)写出仪器名称:a_________;b_________;c_________。
(2)实验室制取二氧化碳所用的药品是__________、___________;
(3)发生装置是_____(填序号);使用该装置还可以制取另一种气体,用化学方程式回答____________。
(4)实验室制取二氧化碳选用的收集装置为___________(填序号)能用该装置收集的气体必须具备的物理性质是_______________________。
(5)如何证明收集的气体是二氧化碳,简述操作步骤和观察到的现象_______________;用化学方程式表示此反应_________________。
(6)假若二氧化碳气体始终不能收集满,可能的一种原因是_____________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(1)请用化学用语表示
① 空气中含量最多的物质 ______;
② 地壳中含量最多的非金属元素是____;
③ 2个亚铁离子________________;
④ 相对分子质量最小的氧化物_______;
⑤ 构成氯化钠的粒子______________。
(2)请用“大于、小于、等于、不大于、不小于或无法确定”填空
① 沸点:液氧 __________ 液氮
② 微粒直径大小:分子____________原子
③ 通常情况下,100毫升酒精与100毫升水混合,总体积__________200毫升。
(3)如图中A、B分别是某微粒的结构示意图,回答下列问题:
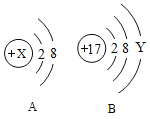
①若A是某阳离子的结构示意图,则x可能是下列中的_______.(填字母序号)
A8 B10 C 11 D12
②若B表示某原子的结构示意图,则y=________.
③若A中x=13,则A、B所表示的元素形成化合物的化学式为_______.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】请你参与实验室配制一定溶质质量分数的硝酸钾溶液的实验,并进行实验过程的探究:
(1)计算:配制50g质量分数为10%的硝酸钾溶液,所需硝酸钾质量为______g,所需蒸馏水的体积为______mL(水的密度约为1g/mL)。
(2)称量:分别在天平左右两盘放上纸片,调节平衡后,应______(填字母序号)。
A先在托盘上放置所需的砝码,再添加硝酸钾直至天平平衡
B先添加所需的硝酸钾,再添加砝码到所在的托盘直至天平平衡
(探究一):在称量过程中,某同学的称量操作如图所示,你认为该操作对本次实验的数据处理的正确性______(填“有”或“没有”)影响,理由是______。
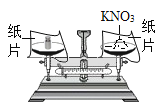
(3)量取:准确量取所需蒸馏水要用到的仪器是____(“少写”或“多写”均不得分)。
(4)溶解:将称量好的硝酸钾和蒸馏水混合溶解。
(探究二):20℃时,将20mL质量分数为10%的硝酸钾溶液,稀释成质量分数为4%的硝酸钾溶液.从表中找出计算所需的密度数据为:______g/mL。
温度℃ 质量分数% | 20 | 40 | 60 |
4 | 1.023 | 1.016 | 1.007 |
10 | 1.063 | 1.054 | 1.044 |
(探究三):已知硝酸钾在部分不同温度时的溶解度如下表
温度/℃ | 20 | 40 | 60 | 80 | 100 |
溶解度/g | 31.6 | 63.9 | 110 | 169 | 246 |
(5)20℃时25 g硝酸钾溶解在50 g水中,所得溶液为______溶液(填“饱和”或“不饱和”),其溶质质量分数为______。
(6span>)将80℃时269g的硝酸钾饱和溶液降温至60℃时(不考虑水分蒸发),所析出晶体的质量是___g。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】近年来随着人们生活水平的提高,汽车已经成为人们主要的出行工具.

(1)汽车的车圈通常使用铝合金材料,是因为铝合金具有___的物理性质(在A、B、C中选).
A 良好导电性 B 抗腐蚀性能好 C 强度硬度较好
(2)铝合金中的金属铝是一种化学性质比较活泼的金属,它不但能与酸反应,还能与氢氧化钠(NaOH)、水反应,生成偏铝酸钠(NaAlO2)和一种可燃性气体单质,请写出此反应的化学反应方程式___铝元素在反应前后的化合价分别是___.
(3)电动汽车以环保、节能的优势日益受到大家的青睐.电动汽车在行驶过程中的能量转化全过程是___.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】小明同学从S+O2![]() SO2中获得以下信息:①该反应反应物是硫和氧气;②反应发生条件是点燃;③反应前后元素种类和原子个数不变;④反应前后分子总数保持不变;⑤参加反应的硫和氧气的质量比为2:1.其中正确的信息是( )
SO2中获得以下信息:①该反应反应物是硫和氧气;②反应发生条件是点燃;③反应前后元素种类和原子个数不变;④反应前后分子总数保持不变;⑤参加反应的硫和氧气的质量比为2:1.其中正确的信息是( )
A. ①②④⑤B. ①②③C. ④⑤D. ①②③⑤
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】现有下列仪器,请你根据所学知识填空:
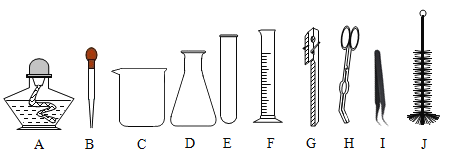
(1)用于少量试剂相互反应所需的容器是___________________;
(2)加热少量水需要用___________________;
(3)量取8.5mL稀盐酸用___________________;
(4)不能加热,不能作反应容器的是___________________.
(5)吸取和滴加少量液体药品用___________________.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】希溪同学在实验室里测定溶液中溶质的质量分数进行了如下实验,他取了锌和硫酸锌的混合物 22.6g,加入了 100g9.8%的稀硫酸,恰好完全反应,然后加入77.6g 水,得到不饱和溶液,流程图如下:
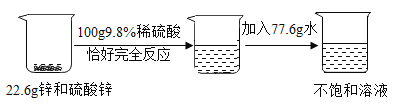
请根据上述内容回答下列问题:
(1)写出反应的化学方程式______________ ;
(2)根据已知条件列出参加反应锌的质量(X)的比例式_____________ ;
(3)反应后所得的不饱和溶液中溶质的质量分数是_______________ ;
(4)上述所用的 100 克 9.8%的稀硫酸是由 98%浓硫酸配制,需加入水的质量是_________;
(5)浓硫酸配成稀硫酸所用的仪器除了烧杯、玻璃棒外,还需的仪器是_____________ 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com