
列溶液无色,在pH=1时能大量共存的是
| A.CuSO4 NaCl KNO3 | B.NaOH NaCl NaNO3 |
| C.Na2SO4 NH4Cl ZnCl2 | D.K2SO4 AgNO3 NaCl |
科目:初中化学 来源: 题型:阅读理解

| 比较项目 | 向上排空气法 | 排水集气法 | 结论 |
| 方法可行性 | O2的密度比空气 |
O2难溶于水且不与水反应 | 两种方法均可行 |
| 收集的过程 | “验满”分析:即便用带火星的木条移近集气瓶口,木条复燃也难以证明空气被排尽,因气体无色,集满与否较难确定. | 集满O2的现象是 |
排水法收集O2更易于观察何时集满 |
| 收集O2的纯度 | 分别用排水法和向上排空气法收集两瓶氧气(A和B),放入两支相同的蜡烛.可观察到B瓶内的蜡烛熄灭较早 |
结论 | |

查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
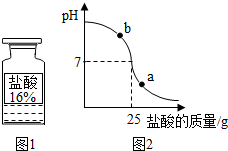 (2013?高淳县二模)学习化学一年后,同学们对课本上“活动性较强的金属一般可以将位于其后面的金属从它们的盐溶液中置换出来”以及“支持燃烧的气体一般是氧气”这两句话产生了质疑.在老师的帮助下,用金属钠来探究下列问题:
(2013?高淳县二模)学习化学一年后,同学们对课本上“活动性较强的金属一般可以将位于其后面的金属从它们的盐溶液中置换出来”以及“支持燃烧的气体一般是氧气”这两句话产生了质疑.在老师的帮助下,用金属钠来探究下列问题:查看答案和解析>>
科目:初中化学 来源:2011-2012学年广东省中山市中考第一次模拟考试化学试卷(解析版) 题型:选择题
列溶液无色,在pH=1时能大量共存的是
A.CuSO4 NaCl KNO3 B.NaOH NaCl NaNO3
C.Na2SO4 NH4Cl ZnCl2 D.K2SO4 AgNO3 NaCl
查看答案和解析>>
科目:初中化学 来源:2013年江苏省南京市高淳县中考化学二模试卷(解析版) 题型:解答题
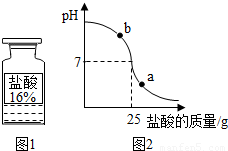
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com