
分析 金属单质、固态非金属单质、稀有气体单质,直接用元素符号表示其化学式;气态非金属单质,在元素符号的右下角写上表示分子中所含原子数的数字.
化合物化学式的书写一般规律:金属在前,非金属在后;氧化物中氧在后,原子个数不能漏,正负化合价代数和为零.
解答 解:氮气属于气态非金属单质,在元素符号的右下角写上表示分子中所含原子数的数字,其化学式为:N2.
碳酸钠中钠元素显+1价,碳酸根显-2价,其化学式为:Na2CO3.
氢氧化铝中铝元素显+3价,氢氧根显-1价,其化学式为:Al(OH)3.
沼气的主要成分是甲烷,其化学式为:CH4.
故答案为:N2;Na2CO3;Al(OH)3;CH4.
点评 本题难度不大,掌握单质(用元素符号或元素符号的右下角写上表示分子中所含原子数的数字)和化合物化学式的书写方法(金属在前,非金属在后;氧化物中氧在后,原子个数不能漏,正负化合价代数和为零)是正确解答此类题的关键.


科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 醋、味精--调味品 | |
| B. | 酒精、汽油--易燃液体 | |
| C. | Na+、Fe3+--人体所需微量元素 | |
| D. | 废塑料瓶、铝制易拉罐--可回收垃圾 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 34.4g | B. | 32g | C. | 18.4g | D. | 9.6g |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
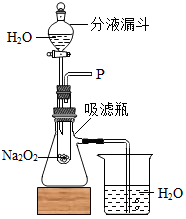 在学校的元旦联欢会上,某同学表演了“水能生火”的魔术.他向包有过氧化钠(Na2O2)粉末的脱脂棉上滴水,脱脂棉燃烧起来.小军很感兴趣,于是,他和同学们进行探究.
在学校的元旦联欢会上,某同学表演了“水能生火”的魔术.他向包有过氧化钠(Na2O2)粉末的脱脂棉上滴水,脱脂棉燃烧起来.小军很感兴趣,于是,他和同学们进行探究.查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
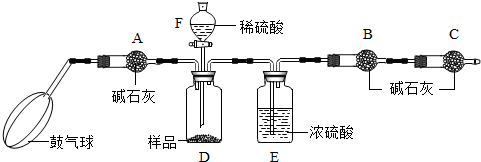
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com