
分析 根据维生素C的缺乏症,蔬菜水果中富含维生素,1个葡萄糖分子的构成,溶质质量=溶液质量×溶质的质量分数,进行分析解答.
解答 解:缺乏维生素C易患坏血病;大枣中富含维生素,食用大枣能为人体提供的主要营养素是维生素.
1个葡萄糖分子是由6个碳原子、12个氢原子和6个氧原子构成的,则碳、氢、氧元素原子个数比是6:12:6=1:2:1.
溶质质量=溶液质量×溶质的质量分数,某患者注射一瓶500克8%的葡萄糖注射液,设需要50%的葡萄糖注射液的质量为x,则
500g×8%=x×50% x=80g.
故答案为:坏血;维生素;1:2:1;80.
点评 本题难度不大,掌握维生素的缺乏症、各种营养素的生理功能与食物来源、化学式的含义、溶质质量=溶液质量×溶质的质量分数是正确解答本题的关键.


科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
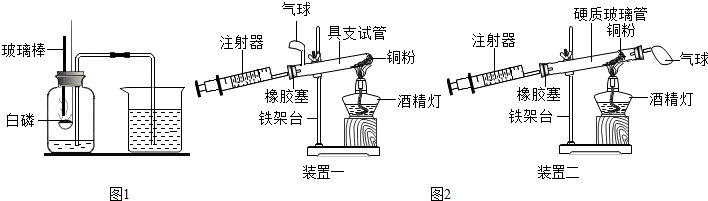
| 硬质玻璃管中空气的体积 | 反应前注射器中空气体积 | 反应后注射器中气体体积 | 实验测得空气中氧气的体积分数 |
| 25mL | 15mL | 9mL |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 如图为A、B、C三种固体物质的溶解度曲线,请根据图示回答下列问题:
如图为A、B、C三种固体物质的溶解度曲线,请根据图示回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | AgNO3、Cu(NO3)2、Fe (NO3 )2 | B. | Cu(NO3)2、Fe (NO3 )2 | ||
| C. | AgNO3、Cu(NO3)2 | D. | Fe (NO3 )2 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 操作 | 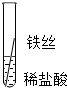 | 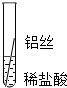 | 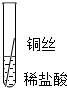 | 根据现象得出金属活动性顺序 |
| 片刻后现象 | 有少量气泡 | 无气泡 | 无气泡 | Fe>Al,Fe>Cu |
| 几分钟后现象 | 有少量气泡 | 有大量气泡 | 无气泡 |
| 操作 | 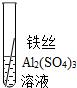 | 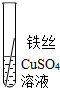 | 根据现象得出金属活动性顺序 |
| 现象 | 无明显现象 | 铁丝表面有红色物质析出 | Al>Fe>Cu |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com