
【题目】我国化学家侯德榜创立的侯氏制碱法为纯碱工业技术发展做出杰出贡献。在制备纯碱过程中涉及Na2CO3、NaCl、NH4Cl、NaHCO3等物质。请结合下表数据回答:
温度/°C | 0 | 10 | 20 | 30 | 40 | 50 | 60 | |
溶解度/g | Na2CO3 | 7 | 12.2 | 21.8 | 39.7 | 48.8 | 47.3 | 46.4 |
NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 | |
NH4Cl | 29.4 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 | 55.2 | |
NaHCO3 | 6.9 | 8.2 | 9.6 | 11.1 | 12.7 | 14.5 | 16.4 | |
(1)在50°C时,向100g水中加入48gNa2CO3充分搅拌所得溶液质量为______,保持烧杯中各物质质量不变,降温至40°C时,所得溶液溶质的质量分数会____(填“变小”、“不变”或“变大”)。
(2)根据表中四种物质的溶解度,回答下列问题:
①60°C时,分别向等质量的四种固体物质中加水配成饱和溶液,所得溶液质量最大的是__。
②侯氏制碱法的原理是:NaCl+NH3+H2O+CO2=NH4Cl+NaHCO3,在生成物碳酸氢钠和氯化铵中,先析出的是_______,理由是_______。
【答案】147.3g 变大 NaHCO3 NaHCO3 反应生成的NaHCO3比NH4Cl质量大,同温度下的NaHCO3溶解度远小于NH4Cl的溶解度
【解析】
(1)由表中数据可知,50℃时,碳酸钠的溶解度是47.3g,即该温度下,100g水中最多能溶解47.3g碳酸钠,故在50°C时,向100g水中加入48gNa2CO3,只能溶解47.3g,充分搅拌所得溶液质量为:100g+47.3g=147.3g;
由表中数据可知,降温至40°C时,溶解度增加,溶质质量增加,所得溶液溶质的质量分数会变大;
(2)①由表中数据可知,60℃时,四种固体物质的溶解度:氯化铵>碳酸钠>氯化钠>碳酸氢钠,故60°C时,分别向等质量的四种固体物质中加水配成饱和溶液,碳酸氢钠所需溶剂的质量最大,即所得溶液质量最大的是碳酸氢钠;
②由表中数据可知,同温度下的NaHCO3溶解度远小于NH4Cl的溶解度,根据化学方程式:![]() ,生成氯化铵和碳酸氢钠的质量比为:53.5:84,故反应生成的NaHCO3比NH4Cl质量大,故碳酸氢钠先析出,理由是:反应生成的NaHCO3比NH4Cl质量大,同温度下的NaHCO3溶解度远小于NH4Cl的溶解度。
,生成氯化铵和碳酸氢钠的质量比为:53.5:84,故反应生成的NaHCO3比NH4Cl质量大,故碳酸氢钠先析出,理由是:反应生成的NaHCO3比NH4Cl质量大,同温度下的NaHCO3溶解度远小于NH4Cl的溶解度。


科目:初中化学 来源: 题型:
【题目】初中化学中的几种常见物质有如图所示的转化关系(部分反应物和生成物已略去),

请回答下列问题:
(1)A的化学式是_____。
(2)反应⑤的化学方程式为_____;
(3)在四种基本反应类型中,如图未涉及到的反应类型是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】据科技部2月15日公布的消息,法匹拉韦(化学式为C5H4FN3O2)是继磷酸氯喹和瑞德西韦之后第三个获准用于治疗新冠肺炎的西药,该药对新冠肺炎的治疗显示出较明显的疗效和较低的不良反应。下列有关法匹拉韦的说法正确的是( )
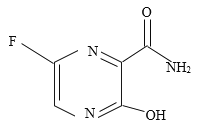
A.法匹拉韦中含有氧分子
B.法匹拉韦的相对分子质量为157g
C.1个法匹拉韦分子由15个原子构成
D.法匹拉韦中氮、氧元素的质量比是3:2
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】水是生命之源,请回答有关水的下列问题:
(1)电解水实验如图所示:
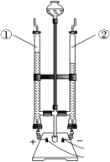
①与②中所得气体的体积比约为_____。该反应的微观示意图如下,请在方框内补全相应微粒的示意图_____。
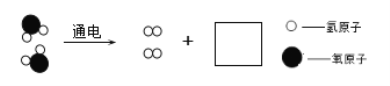
(2)“生命吸管”是一种便携式户外净水器。其净水原理如下图:
![]()
①过滤网可去除_____(填“可溶性”或“难溶性”)杂质。
②抗菌活性复合滤料中有活性炭、离子交换树脂等。活性炭所起的是_____作用。离子交换树脂能去除原水中的钙离子,钙离子的符号是_____。
(3)如图是A、B、C三种固体物质的溶解度曲线图,请结合图示回答下列问题:
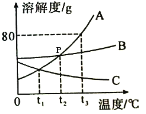
①p点的含义是_____。
②室温下,将盛有A的饱和溶液的试管放入盛水的烧杯中,再向烧杯内的水中加入一定量的并NH4NO3并搅拌,试管内可观察到的现象是_____。
③将t3℃时A、B、C三种物质的饱和溶液降温到t1℃,所得溶液中溶质的质量分数的由大到小的关系是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】有趣的“纳米小人”是一系列结构式与人体相似的有机分子(化学式C39H42O2),是由莱斯大学的詹姆斯·托尔等人设计并合成分子,用于对年轻学生的化学教育,下列关于它的说法中正确的是( )
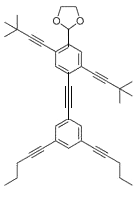
A.“纳米小人”中碳元素的质量分数约为86.3%
B.“纳米小人”是由碳、氢两个元素组成的
C.“纳米小人”中氢、氧元素的质量比为21:1
D.“纳米小人”的相对分子质量为532
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】硅晶体广泛应用于电子工业的各个领域,工业上常用焦炭在高温下还原二氧化硅固体初步制得,主要反应为:SiO2+2C![]() Si+2CO↑,求:
Si+2CO↑,求:
(1)二氧化硅中硅元素的质量分数_________;
(2)要生产含硅质量分数为90%的粗硅2.8吨,计算至少需要焦炭______吨?
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】小瑾同学按如图所示进行了有关金属性质的探究实验。下列有关说法中,正确的是( )
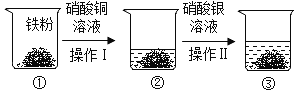
A.烧杯②中的固体一定为铜和铁的混合物
B.烧杯②中的溶液可能含有两种溶质
C.烧杯③中的溶液中,一定含有Fe2+、Cu2+、Ag+
D.烧杯③中的固体质量一定大于烧杯②中的固体质量
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】Ⅰ.配制一定溶质质量分数的氯化钠溶液的过程如图所示:
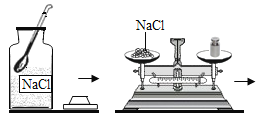
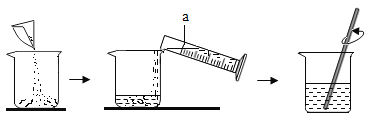
(1)写出图中标号a仪器的名称____________。
(2)称量氯化钠时,氯化钠应放在托盘天平的______________盘。 (填“左”成“右”)
(3)对配制的溶液进行检测发现溶质质量分数偏小,其原因可能有_____________ (填序号)
A 称量时,药品与砝码放反了
B 量取水的体积时,仰视读数
C 装瓶时,有少量溶液洒出
(4)把50g质量分数为15%的氯化钠溶液稀释成5%的氯化钠溶液,需要水的质量是_____________g.
Ⅱ.除去粗盐中难溶性杂质后,得到的固体中除了NaCl还含有少量的可溶性杂质MgCl2、CaCl2,某同学为除去可溶性杂质,将该固体加水溶解形成溶液A.并设计如下方案:
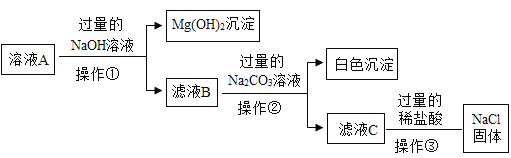
(1)操作①、操作②指的是_______________;
(2)滤液B中的溶质是_______________;
(3)加入过量的NaOH溶液发生反应的化学方程式为_______________;
(4)操作③中加过量的稀盐酸的目的是_______________.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】为了测定一瓶硫酸铜溶液的溶质质量分数,取出50克该溶液,向其中逐滴加入溶质质量分数为16%的氢氧化钠溶液,反应过程中生成沉淀的质量与所用氢氧化钠溶液质量的关系如图所示:
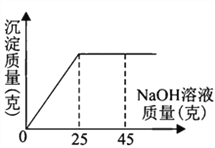
请你仔细分析此关系图,并进行计算。
(1)当滴入氢氧化钠溶液_____克时,硫酸铜与氢氧化钠恰好完全反应。
(2)计算此硫酸铜溶液中溶质的质量分数为_________(写出计算过程)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com