
【题目】某小组用粗锌测定某稀硫酸中溶质的质量分数。取一定质量的稀硫酸于烧杯中,称量稀硫酸和烧杯的总质量;然后,向其中分两次加入粗锌(杂质不参加反应),实验过程和数据如图所示。请计算:
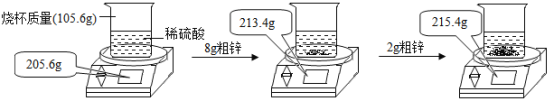
(1)生成氢气的总质量为 g。
(2)稀硫酸中溶质的质量分数。
科目:初中化学 来源: 题型:
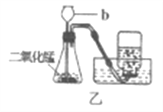
【题目】同学们做粗盐提纯(如图甲)和制取氧气实验(如图乙)。请回答下列问题:
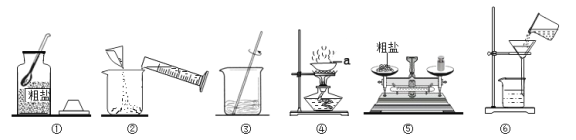
(1)仪器a的名称是__________。
(2)有一处操作存明显错误的,请你改正_______________。
(3)正确的操作顺序是________(填操作序号),以及称量精盐并计算产率。
(4)使用仪器b在该实验中的优点是______,写出乙装置中反应的化学方程为________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列图像能正确反映对应变化关系的是( )
A.向一定量的过氧化氢溶液中加入少量二氧化锰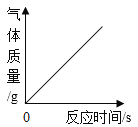
B.在密闭容器中用足量红磷测定空气中氧气的含量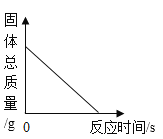
C.向一定量的氯化铜和稀盐酸的混合溶液中滴加氢氧化钡溶液
D.向一定量的铜粉中加入硝酸银溶液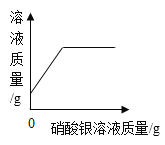
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是甲、乙、丙三种固体物质的溶解度曲线。
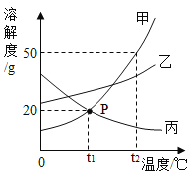
(1)P点表示的含义为_______。
(2)t1℃时,60g甲物质的饱和溶液升温到t2℃,再加_____g甲物质,溶液仍然饱和。
(3)t2℃时,甲溶液中有少量丙,要提纯甲,用_____结晶法。
(4)将t2℃时的甲、乙、丙的饱和溶液降温到t1℃,所得溶液中溶质的质量分数由大到小的顺序为______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】向盛有一定量铜和氧化铜混合物的烧杯中滴加稀盐酸,边滴边搅拌,反应过程中剩余固体的质量与加入稀盐酸的质量关系如图所示。下列说法不正确的是
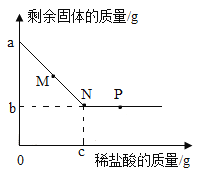
A.M点时,剩余固体是铜和氧化铜
B.M、N点时,溶液中的溶质均只有CuCl2
C.N、P点时,溶液的pH:N>P
D.混合物中铜的质量为(a-b)g
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某班同学用氢氧化钠溶液和稀硫酸进行中和反应实验:
(1)甲同学在烧杯中加入约5mL氢氧化钠溶液,滴入几滴无色酚酞溶液,此时溶液呈_____色,接着用滴管滴入一定量的稀硫酸,再用玻璃棒搅拌,发现溶液变为无色,该反应的化学方程式为_____
(2)甲、乙、丙同学对反应后溶液中的溶质成分进行探究。
(猜想与假设)反应后溶液中的溶质是什么?
猜想一:只有Na2SO4;
猜想二:_____
猜想三:可能是Na2SO4和NaOH
以上猜想中,可以直接排除的是_____,理由_____。
(实验探究)
为了验证另外两种猜想,甲、乙、丙同学设计如下实验方案:
实验操作 | 实验现象 | 实验结论 | |
甲同学方案 | 取少量反应后的溶液于试管中,向试管中滴加BaCl2溶液, | 有白色沉淀产生。 | 猜想二成立 |
乙同学方案 | 取少量反应后的溶液于试管中,向试管中加入_____ | 有气泡产生。 | 猜想二成立 |
丙同学方案 | 取少量反应后的溶液于试管中,向试管中加入生锈的铁钉。 | _____ | 猜想二成立 |
老师认为甲同学方案不合理,你认为理由是_____。
(反思交流)实验结束后,废液处理方法正确的是_____(填序号)。
A 倒入下水道 B 倒入废液缸
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】2020年3月26日,科技部长徐南平指出,我国已经筛选出磷酸氯喹、法匹拉韦、可利霉素等药物,在临床中显示这些药物治疗新冠肺炎有一定的疗效。其中磷酸氯喹的化学式为![]() ,下列有关磷酸氯喹的说法错误的是( )
,下列有关磷酸氯喹的说法错误的是( )
A.磷酸氯喹是一种有机物
B.一个磷酸氯喹分子含有64个原子
C.磷酸氯喹由碳、氢、氯、氮、氧、磷六种元素组成
D.磷酸氯喹中碳、氢、氮三种元素的质量比为18:32:3
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】第32届夏季奥运会将在日本东京举行,其奖牌制作的原料来自于电子垃圾中提炼出来的金属。从废线路板中提炼贵重金属和制备硫酸铜晶体的一种工艺流程如下:
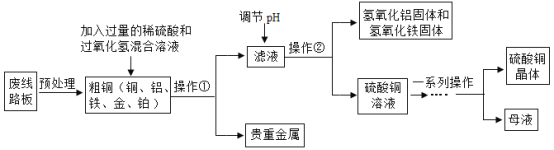
已知:在酸性环境中有过氧化氢存在时,铁和铜分别会转化为铁离子和铜离子。
(1)操作②的名称是________;
(2)提炼出的贵重金属可制作奖牌,其成分是______________;
(3)“调节pH”时加碱液会使溶液的pH________(填“增大”或“减小”),其主要目的是除去滤液中Al3+和______(填金属离子符号);
(4)写出粗铜中的铜与稀硫酸和过氧化氢的混合溶液发生反应的化学方程式:__________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com