
| 甲 | 乙 | 丙 | |
| 金属混合物的质量(g) | 10 | 10 | 20 |
| 稀硫酸质量(g) | 100 | 120 | 100 |
| 反应后余下固体质量(g) | 2 | 2 | 12 |
| 8g |
| 10g |
| 56 |
| 8g |
| 152 |
| x |
| 56 |
| 8g |
| 98 |
| y |
| 14g |
| 100g |


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:
| A、用食醋鉴别食盐和纯碱 |
| B、用酚酞试液鉴别稀硫酸与氯化钠溶液 |
| C、用灼烧方法鉴别羊毛和合成纤维 |
| D、用熟石灰鉴别铵态氮肥和钾肥 |
查看答案和解析>>
科目:初中化学 来源: 题型:
 2013年11月4日哈尔滨再次出现雾霾天气,空气质量污染综合指数AQI超过340以上,PM2.5达到300以上.PM2.5是指直径小于或等于2.5微米的微粒物,它的直径还不到人头发丝粗细的
2013年11月4日哈尔滨再次出现雾霾天气,空气质量污染综合指数AQI超过340以上,PM2.5达到300以上.PM2.5是指直径小于或等于2.5微米的微粒物,它的直径还不到人头发丝粗细的| 1 |
| 20 |
查看答案和解析>>
科目:初中化学 来源: 题型:
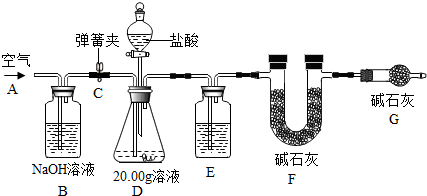
查看答案和解析>>
科目:初中化学 来源: 题型:
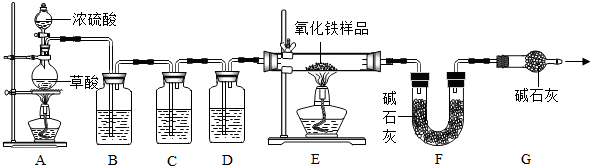
| ||
| △ |
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
| 实验操作 | 预期现象与结论 |
查看答案和解析>>
科目:初中化学 来源: 题型:

查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com