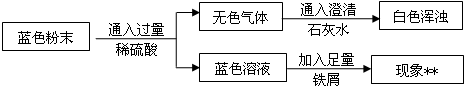
15、某研究性学习小组对“H
2S的水溶液是否显酸性”进行探究.请你参与他们的探究活动,并回答有关问题.
(1)查阅资料:①H
2S是一种无色、有臭鸡蛋气味的有毒气体,能溶于水,在常温常压下,1体积水中能溶解2.6体积硫化氢;密度比空气的大;②实验室里,通常用硫化亚铁(FeS)固体跟稀盐酸或稀硫酸反应制取硫化氢.
(2)提出假设:H
2S的水溶液显酸性
(3)实验探究:
I.制备H
2S

①若用稀盐酸制备H
2S,其化学方程式为
FeS+2HCl═FeCl2+H2S↑
.
②制取H
2S的发生装置为
A
(填字母),收集装置只能选D的原因是
H2S溶于水且密度比空气大
.
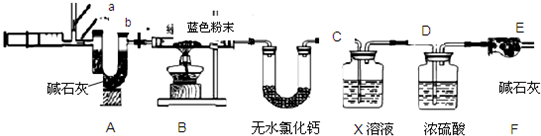
II.设计如下图所示装置进行验证实验.

(1)实验过程中,A装置内蓝色石蕊试纸的颜色始终没有变化.A装置的作用是
证明H2S气体不能使蓝色石蕊试纸变色
.
(2)在通入H
2S之前将B装置中胶头滴管内的蒸馏水滴到蓝色石蕊试纸上,未见试纸颜色发生变化,此操作的目的是
证明水不能使蓝色石蕊试纸变色
.当有H
2S通过时发现湿润的蓝色石蕊试纸变红,此现象说明
硫化氢的水溶液显酸性
.
(3)结论:原假设成立.
(4)反思与评价:该验证实验中,有一个明显疏漏,请你指出疏漏之处为
没有尾气处理(或吸收)装置
.
(5)知识拓展:H
2S的水溶液显酸性,具有酸的通性,若用氢氧化钠溶液吸收尾气,则反应的化学方程式为
2NaOH+H2S=Na2S+2H2O
.





 阅读快车系列答案
阅读快车系列答案