
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量溶液于试管,加稀盐酸. | 有气泡冒出 | 该溶液是碳酸钠溶液.有关反应的化学方 程式为Na2CO3+2HCl═2NaCl+H2O+CO2↑ |
分析 (1)根据氢氧化钙溶解度与饱和溶液的溶质质量分数的关系进行分析解答.
(2)根据溶液pH值的测定方法进行解答;
(3)根据碳酸钠能和盐酸反应放出二氧化碳气体以及碳酸钠能和氢氧化钙溶液反应生成碳酸钙沉淀和氢氧化钠进行解答;
(4)根据碳酸钙的质量求出碳酸钠的质量,进而求出该纯碱样品中碳酸钠的质量分数即可;
(5)根据探究方案中因缺少干燥导致碳酸钠的质量分数偏大进行解答.
解答 解:(1)常温下氢氧化钙的溶解度为0.18g,其饱和溶液中溶质质量分数=$\frac{0.18g}{100g+0.18g}$×100%<0.18%,而该溶液溶质质量分数为10%,故不可能是氢氧化钙;
(2)测定溶液的pH值,不能将pH试纸湿润,否则会使得溶液的酸碱性变弱,测碱溶液使pH值偏小,所以用洁净干燥的玻璃棒蘸取该溶液滴到湿润的pH试纸上,测得pH=10,判断该溶液中不可能是氯化钠,方法不正确,结果偏小,但结论正确;
(3)碳酸钠能和盐酸反应放出二氧化碳气体,所以试验方法:
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量溶液于试管,加稀盐酸. | 有气泡冒出 | 该溶液是碳酸钠溶液.有关反应的化学方 程式为Na2CO3+2HCl═2NaCl+H2O+CO2↑ |
点评 本题难度较大,可采取“利用测定结果进行先排除,最后进行实验检验”的思路确定未知溶液,解题的关键是熟练掌握氢氧化钠、氯化钠、氢氧化钙、碳酸钠的性质.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
 根据如图所示实验回答:
根据如图所示实验回答:查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
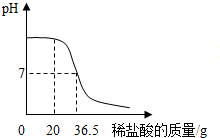 某化学兴趣小组在实验室配制一定溶质质量分数的稀盐酸,并用其测定某氢氧化钠溶液的溶质质量分数.
某化学兴趣小组在实验室配制一定溶质质量分数的稀盐酸,并用其测定某氢氧化钠溶液的溶质质量分数.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 倾倒液体时,试剂瓶口紧挨着试管口快速倒入 | |
| B. | 加热蒸发过程中,当溶液蒸干时停止加热 | |
| C. | 用pH试纸测定溶液的酸碱度时,将pH试纸放入待测液中蘸取 | |
| D. | 过滤时,漏斗中液面低于滤纸的边缘 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com