
| 温度 | NH4Cl | NH4HCO3 | NaHCO3 | NaCl |
| 30℃ | 41.1g | 27.0g | 11.1g | 36.3g |
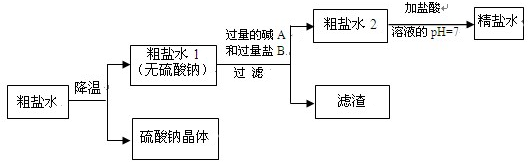
分析 (1)根据化学反应反应物和生成物的种类即可判断反应的类型进行解答;
(2)①根据硫酸钠的溶解度随温度变化明显而氯化钠的溶解度受温度变化不明显进行解答;
②要除去粗盐中含有的氯化镁,可以加入氢氧化钙进行解答;
③要除去氯化钙可以加入碳酸钠,加入的碳酸钠能与过量的氢氧化钙反应,加入的B盐为碳酸钠进行解答;
④根据第二步食盐与NH4HCO3反应是复分解反应,以及碳酸氢钠的溶解度较小的信息书写方程式.
解答 解:(1)NH3+CO2+H2O=NH4HCO3中,反应物有三种,生成物是一种,所以属于化合反应;
(2)①硫酸钠的溶解度随温度变化明显而氯化钠的溶解度受温度变化不明显,所以从粗盐水中析出硫酸钠晶体其原理是降温结晶;
②要除去粗盐中含有的氯化镁,可以加入氢氧化钙生成氯化钙和氢氧化镁沉淀,化学方程式为:Ca(OH)2+MgCl2=Mg(OH)2↓+CaCl2;
③要除去氯化钙可以加入碳酸钠,加入的碳酸钠能与过量的氢氧化钙反应,加入的B盐为碳酸钠,反应后生成碳酸钙沉底和氢氧化镁沉淀,所以滤渣中含有的物质是Mg(OH)2、CaCO3;
④食盐与NH4HCO3反应是复分解反应,根据反应特点“两交换,价不变”判断,产物是氯化铵和碳酸氢钠,碳酸氢钠的溶解度较小,易结晶析出,可视为沉淀,化学方程式为:NH4HCO3+NaCl=NaHCO3↓+NH4Cl.
故答案为:(1)化合反应;
(2)①降温结晶;
②Ca(OH)2+MgCl2=CaCl2+Mg(OH)2↓;
③Na2CO3,CaCO3、Mg(OH)2;
④NH4HCO3+NaCl=NaHCO3↓+NH4Cl.
点评 本题考查了碳酸钠的制取,完成此题,可以依据题干提供的信息结合已有的知识进行,难度较大.


科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 铁丝在氧气中燃烧时集气瓶瓶底炸裂--红热的铁丝碰到集气瓶内壁 | |
| B. | 向澄清石灰水中通入二氧化碳无明显现象--可能是二氧化碳中混有氯化氢气体 | |
| C. | 将表面未处理的铝丝插入硫酸铜溶液中无明显现象--铝的金属活动性比铜弱 | |
| D. | 在粗盐提纯实验中过滤速率过慢--没用玻璃棒引流 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 温度/℃ | 10 | 20 | 30 | 40 | |
| 溶解度/g | 氯化钠 | 35.8 | 36.0 | 36.3 | 36.6 |
| 碳酸钠 | 12.2 | 21.8 | 39.7 | 53.2 | |

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 给烧瓶、烧杯里的固体物质加热时,一定要垫上石棉网,防止受热不均而炸裂 | |
| B. | CO还原CuO实验结束时,先熄灭酒精灯,冷却后再停止通CO,防止红热的铜被氧化 | |
| C. | 稀释浓硫酸时,要将水沿烧杯内壁缓慢注入浓硫酸中,并用玻璃棒不断搅拌 | |
| D. | 测溶液的PH时,用玻璃棒蘸取待检液涂在湿润后的PH试纸上,再与比色卡对比读数 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题

| A. | 甲实验的步骤是①④⑤,其中除杂质的关键步骤是蒸发 | |
| B. | 甲实验④中,玻璃棒的作用是搅拌加快过滤速度 | |
| C. | 乙实验若按②③①的步骤进行操作,所配溶液的浓度会偏小(水的密度为1g/cm3) | |
| D. | 乙实验②中,若左盘放砝码,右盘放药品,所称得的氯化钠一定比实际需要量少 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
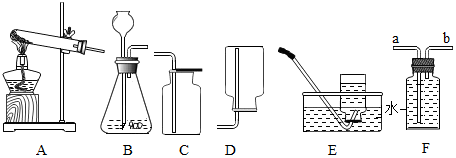
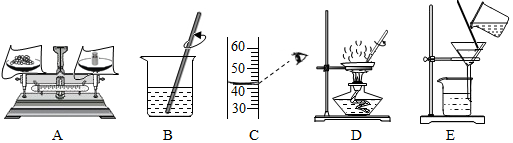
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com