
【题目】请结合图示实验装置,回答下列问题.
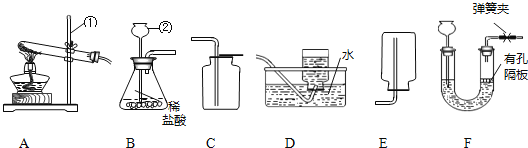
(1)标号②的仪器名称:_____.
(2)实验室制取CO2反应的化学方程式为_____.如何检验该气体为CO2_____.
(3)实验室可用(NH4)2SO4固体和熟石灰混合加热制取NH3,NH3易溶于水,实验室制取NH3应选择的装置为_____(选填序号),其发生装置选择的依据是_____.
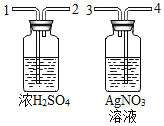
(4)兴趣小组选用F制氢气,其优点是_____,为了检验并除去杂质,得到纯净、干燥的H2,除杂装置(如图)的导管按气流方向连接顺序是_____(选填字母)
A 1→2→4→3 B 2→1→3→4
C 4→3→1→2 D 3→4→2→1.
【答案】长颈漏斗 CaCO3+2HCl═CaCl2+H2O+CO2↑ 将气体通入澄清的石灰水中,若变浑浊,则为二氧化碳 AE 反应物是固体,反应条件是加热 能够随时控制反应的进行或停止 C
【解析】
(1)据图可知标号②的仪器是长颈漏斗;
(2)碳酸钙和稀盐酸反应生成氯化钙、水和二氧化碳,化学方程式为:CaCO3+2HCl═CaCl2+H2O+CO2↑;二氧化碳气体用澄清石灰水进行检验,将气体通入澄清的石灰水中,若变浑浊,则为二氧化碳;
(3)实验室可用(NH4)2SO4固体和熟石灰固体混合加热制取NH3,故选择加热固体产生气体的A装置作为发生装置,NH3是一种密度小于空气,极易溶于水的气体,故选择向下排空气法收集氨气;
(4)选用F装置制取氢气,其优点是能够随时控制反应的进行或停止;二氧化碳气体中常含有少量HCl和水蒸气,为了制得纯净、干燥的二氧化碳气体,应先把混合气体通入碳酸氢钠的饱和溶液除去氯化氢气体,再通过浓硫酸除去水蒸气,因此连接顺序是:4→3→1→2。


科目:初中化学 来源: 题型:
【题目】工业盐酸中通常因溶有少量的 FeCl3而呈黄色,小红为测定某工业盐酸中 HCl 的含量进 行如下实验:取某工业盐酸 l00g,滴加一定溶质质量分数的 NaOH 溶液,测得加入 NaOH溶液质量与反应生成的沉淀质量关系如图所示,FeCl3与 NaOH 反应的化学方程式为FeCl3+3NaOH═Fe(OH)3↓+3NaCl.请回答下列问题:
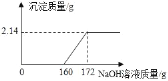
(1)FeCl3与 NaOH 恰好完全反应时,生成沉淀的质量是_____ g;
(2)所滴加的 NaOH 溶液质量为 160 克时,溶液中的溶质是_____;
(3)该工业盐酸中 HCl 的质量分数是多少?_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验室中同学们进行了如图所示实验,成功探究出了久置氢氧化钠固体的变质情况。下列说法正确的是( )
![]()
A. 甲溶液可以选择稀盐酸或CaC12溶液(查阅资料得知:CaC12溶液显中性)
B. 若Ⅱ、Ⅲ均有明显现象,则说明样品部分变质
C. D物质可能是气体,也可能是沉淀
D. 溶液B中的溶质一定只含有NaOH和甲
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验室用铜辉矿(主要成分为Cu2S,含少量Fe2O3、SiO2等杂质,SiO2不与酸反应)制备碱式碳酸铜(Cu2(OH)2CO3)的主要实验流程如图。
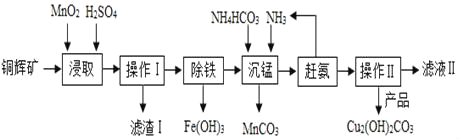
(1)Cu2S中铜元素的化合价_____。
(2)“浸取”步骤中发生反应(I、II),其中反应I为:2MnO2+Cu2S+□H2SO4=2MnSO4+2CuSO4+S↓+4H2O,请在□中填上合适的化学计量数为_____。
(3)“浸取”步骤中,另一反应II为_____。
(4)滤渣I的成分为MnO2、S、_____。
(5)赶走氨的实验操作方法是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】将氯化钠和硫酸钠固体混合物共15g完全溶于水后,加入一定质量分数的氯化钡溶液208g,恰好完全反应,过滤、洗净、烘干得到23.3g沉淀。计算:
(1)所加氯化钡溶液的溶质质量分数;
(2)原固体混合物中氯化钠的质量。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】为了研究可燃物的燃烧条件,某兴趣小组同学用如图所示装置进行了实验(白磷、红磷均不超过绿豆大小,锥形瓶中的白磷A与红磷C尽量拉开距离)。白磷的着火点为40℃,红磷的着火点为240℃。

(1)写出锥形瓶中发生的实验现象:______________。
(2)结合本实验目的,写出烧杯70℃热水的作用:______________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】今年我市化学实验操作考察的实验之一是“高锰酸钾制取氧气”.现摘录某同学的实验过程如下:
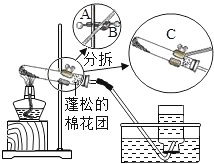
①选择适当仪器,组装成如图所示的实验装置;
②检查装置气密性,装置气密性良好;
③向集气瓶中加水,并倒置于盛有水的水槽中,集气瓶底部出现气泡;
④将药品平铺于干燥试管底部,在导管口放置蓬松的棉花团,塞上橡皮塞,固定于铁架台上;
⑤点燃酒精灯加热,待导管口有气泡产生,立即用集气瓶进行收集;
⑥气体收集完毕,用毛玻璃片将集气瓶口盖好,从水中取出并正放在桌面上;
⑦先熄灭酒精灯,后将导管从水槽中取出;…
请回答下列问题:
(1)写出用高锰酸钾制氧气的化学方程式:_____;
(2)欲调整试管高度,应调节图中A、B、C哪个旋钮:_____;
(3)步骤②的操作与观察到的现象是:_____;若装置无破损,加热一段时间后,观察到高锰酸钾已大量分解,但导管口仍未产生明显气泡,可能的原因是_____;
(4)上述实验步骤中,可能导致集气瓶中收集的氧气不纯净(水蒸气不计)的是_____;(填序号)
(5)步骤⑦中的操作,可能引起_____.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】近年各大体坛赛事报道频繁出现一个名词“嗅盐”。某校兴趣小组在老师的指导下,对“嗅盐”展开了系列探究:
(查阅资料)①嗅盐,是一种由碳酸铵和香料配制而成的药品,给人闻后有刺激作用;
②嗅闻原理是碳酸铵晶体产生的氨气对人体有刺激作用,过量嗅闻不利健康;
③碳酸铵[(NH4)2CO3]晶体受热易分解,产生 NH3、H2O、CO2。
(定性初探)验证“嗅盐”的化学性质
(1)甲同学进行了NH4+的验证实验:取适量嗅盐于试管中,加入氢氧化钠溶液共热,在试管口放一张_____,观察到了预期的实验现象。请写出氢氧化钠溶液与碳酸铵反应的化学方程式_____。
(2)乙同学进行了 CO32﹣的验证实验:取适量嗅盐于试管中,再加入稀硫酸,并将生成的气体通入_____,预期的实验现象是_____,实验后观察到了预期的现象。
(定量再探)测定“嗅盐”中碳酸铵(NH4)2CO3的质量分数
方案Ⅰ:取样品 6.0 克,用图 1 装置进行实验,测量C装置在反应前后增加的质量即为产生NH4+的质量:
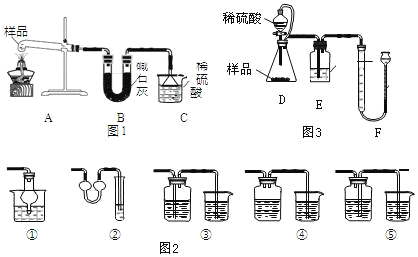
(3)装置B的作用_____,装置C中普通漏斗的作用是_____,图2装置中不能与其起到相似作用的是_____。
(4)小组同学经讨论后,均认为用该套装置测量会导致碳酸铵的质量分数偏小,原因是_____。
方案Ⅱ:取样品6.0克,用图3装置进行实验,利用F装置测量反应生成气体的体积。
(5)请写出装置D中发生反应的化学方程式_____,装置 D 中橡胶管除平衡压强,便于液体顺利滴下外,还有_____的作用。
(6)该方案实验结束后,会有气体残留,不能完全进入量气管中,_____(填“需要”或“不需要”)通入N2将其 中残留的气体排入量气管中,阐述你的理由_____。
(7)实验测得量气管中产生气体的体积为 558mL,该方案所测嗅盐中碳酸铵的质量分数为_____。(已知实验条件下,CO2的密度约为 1.97g/L)。(请写出过程,计算结果精确到 1%)
(8)若其他操作均正确,下列因素会导致所测嗅盐中碳酸铵的质量分数偏大的是_____ (填字母)
a反应前量气管液面在 0 刻度处以下
b实验结束后,调节两端液面相平读数
c反应结束后未等装置冷却到室温,就开始读数
d反应前正确读取量气管中液体体积,反应后仰视读数
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】氯化钙在生活中常用作干燥剂、融雪剂,在工业上可用于制造防冻液等。某工厂以石灰石为原料生产氯化钙晶体的流程如下:(原料石灰石中含的杂质主要是MgCO3、MgSO4 和Al2O3) 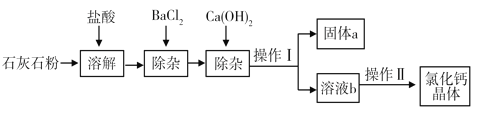
(1)石灰石粉溶解时,Al2O3发生反应的化学方程式为_____________________;
(2)加入BaCl2除杂的化学方程式为_____________________________;
(3)操作Ⅱ的具体步骤为___________________ 、冷却结晶;
(4)固体a的成分中含有的物质有_________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com